CAPAとは!?
CAPA(キャパ)とは!?
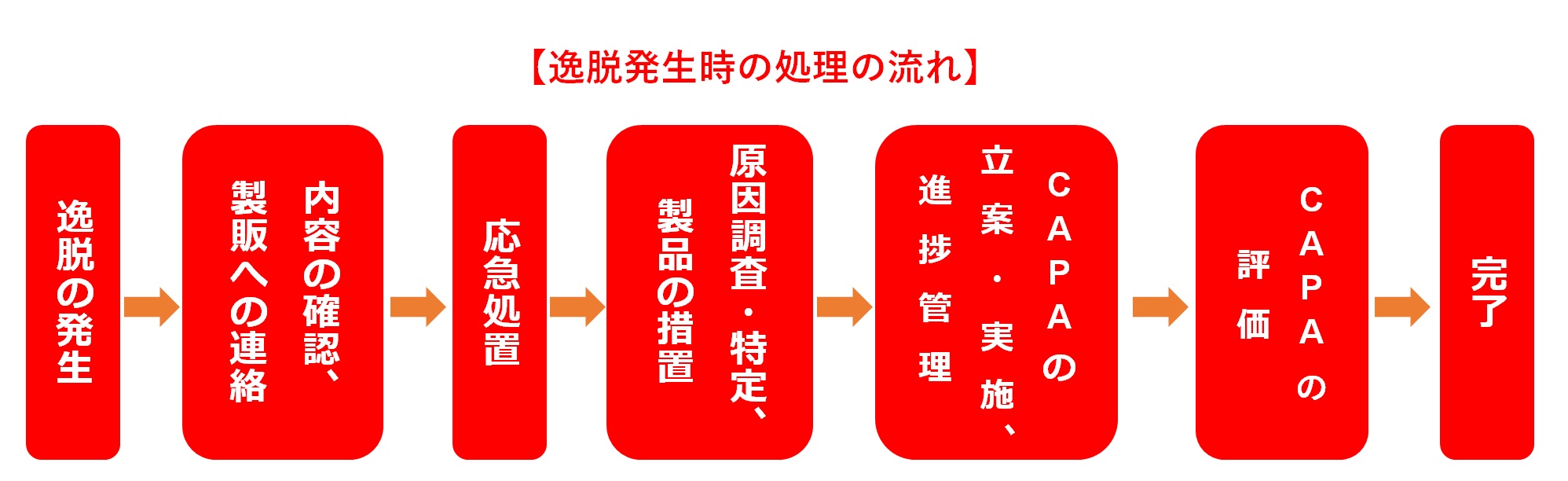
CAPA(キャパ)とは…Corrective Action and Preventive Actionの略称であり、日本語では「是正処置・予防処置」と訳される。
CAPAは、GMP(医薬品の製造管理及び品質管理の基準)やISO 13485(医療機器産業の品質マネジメントシステム)において、品質システムを継続的に改善するための最重要プロセスである。
不適合(逸脱や苦情等)が発生した際に、単にその場を収める(修正)だけでなく、根本原因を除去し、二度と同じ問題を繰り返さない(是正)、あるいは未然に防ぐ(予防)ための体系的な手順を指す。
【CAPAの本質】
CAPAは単なる「問題解決ツール」ではない。組織が自ら学習し、システムそのものを進化させるための「成長エンジン」である。品質部門だけでなく、経営層から現場作業者まで、全員がこのサイクルを意識することが、強い品質文化(Quality Culture)を築く鍵となる。
「修正」「是正」「予防」の決定的な違い
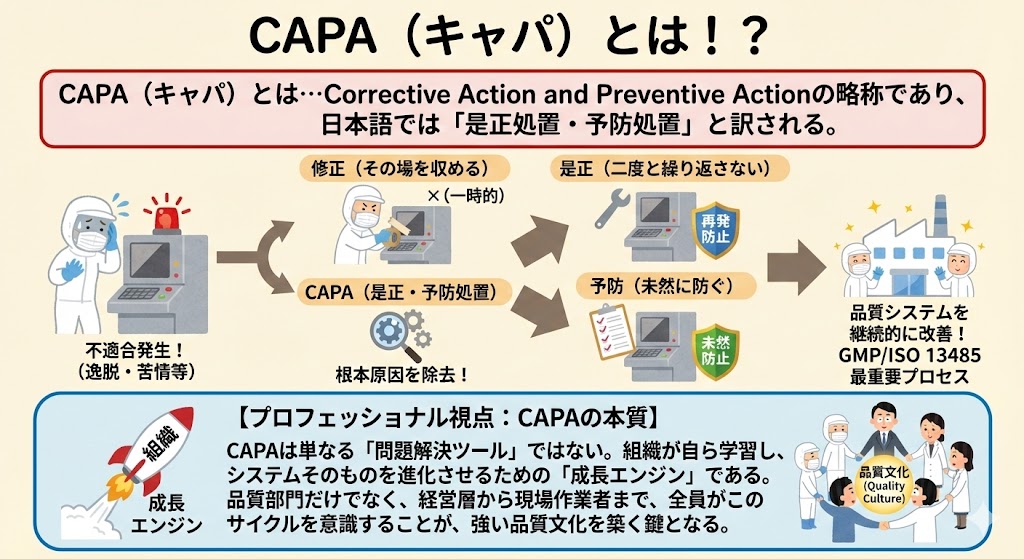
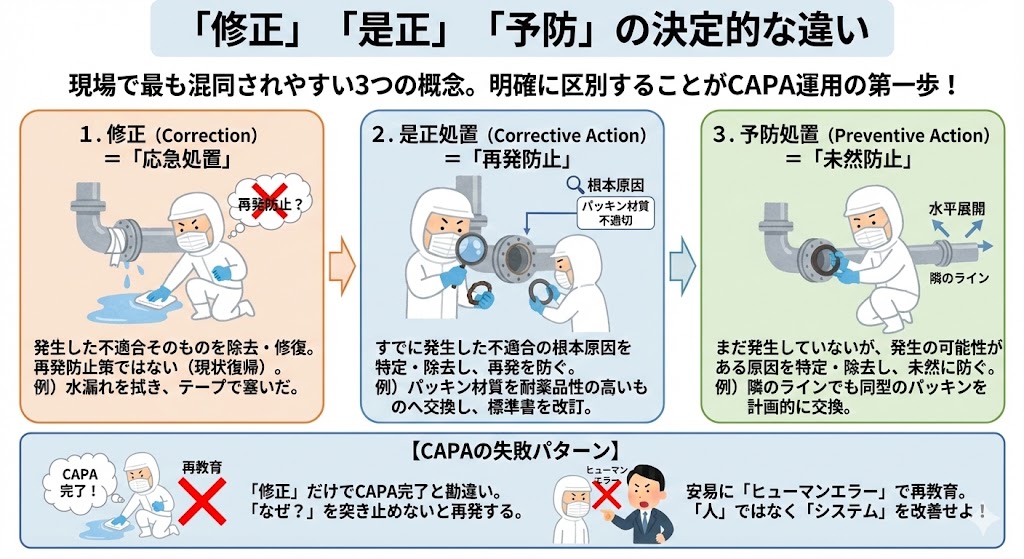
現場で最も混同されやすいのが、これら3つの概念である。これらを明確に区別することが、CAPA運用の第一歩である。
1、修正(Correction)=「応急処置」
発生した不適合そのものを除去・修復する措置。再発防止策ではない。
例)配管から水漏れが発生したため、こぼれた水を拭き取り、テープで穴を塞いだ。
(※これはCAPAの入り口であり、CAPAそのものではない。あくまで現状復帰である)
2、是正処置(Corrective Action)=「再発防止」
すでに発生した不適合の根本原因(Root Cause)を特定し、除去することで、再発を防ぐ措置。
例)なぜ穴が開いたか調査したところ、パッキンの材質が流体に不適切で劣化が早まったことが判明した。そのため、耐薬品性の高い材質のパッキンへ交換し、標準書の材質指定を改訂した。
3、予防処置(Preventive Action)=「未然防止」
まだ発生していないが、発生する可能性がある不適合の潜在的な原因を特定し、除去することで、発生を未然に防ぐ措置。他ラインや他製品への水平展開が含まれる。
例)隣のラインでも同種の流体を扱う配管を使用しているため、漏れは起きていないが、同様に耐薬品性の高いパッキンへの交換を計画的に実施した。
【CAPAの失敗パターン】
多くの現場で、「修正(応急処置)」を行っただけで「是正(CAPA)」が完了したと勘違いするケースが見受けられる。「水を拭いた(修正)」だけでは、明日また水は漏れる。「なぜ漏れたのか?」を突き止めない限り、CAPAは完了しない。
また、根本原因を安易に「担当者の不注意(ヒューマンエラー)」と結論付け、「再教育を行う」という是正処置でお茶を濁すことも避けるべきである。それは「人」の問題であり、根本的な「システム(仕組み)」の改善になっていないからである。人が間違えない仕組みを作ることが真の是正処置である。
CAPAの流れ(7ステップ)
効果的なCAPAを実施するための一般的なフローは以下の通りである。
1.不適合の明確化(事実確認・5W1H)
2.修正(応急処置・拡大防止・リスク評価)
3.根本原因分析(Root Cause Analysis:なぜなぜ分析、特性要因図等)
4.是正処置・予防処置の計画立案
5.処置の実施
6.有効性の評価(処置が適切だったか、再発していないかを確認)
7.完了・横展開(標準書への反映、他部署への共有)
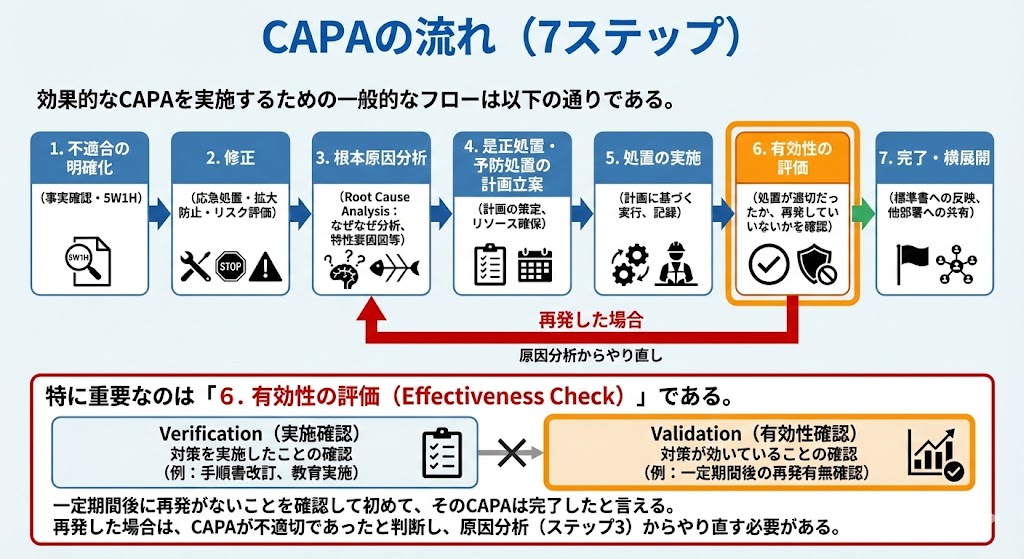
特に重要なのは「6.有効性の評価(Effectiveness Check)」である。「対策を実施したこと(Verification)」と「対策が効いていること(Validation)」は別物である。一定期間後に再発がないことを確認して初めて、そのCAPAは完了したと言える。再発した場合は、CAPAが不適切であったと判断し、原因分析(ステップ3)からやり直す必要がある。