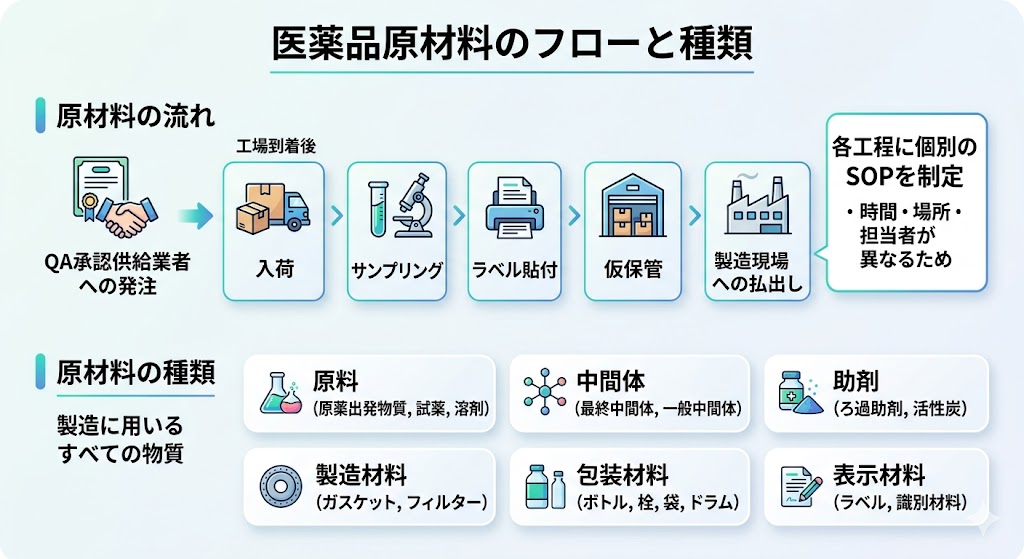
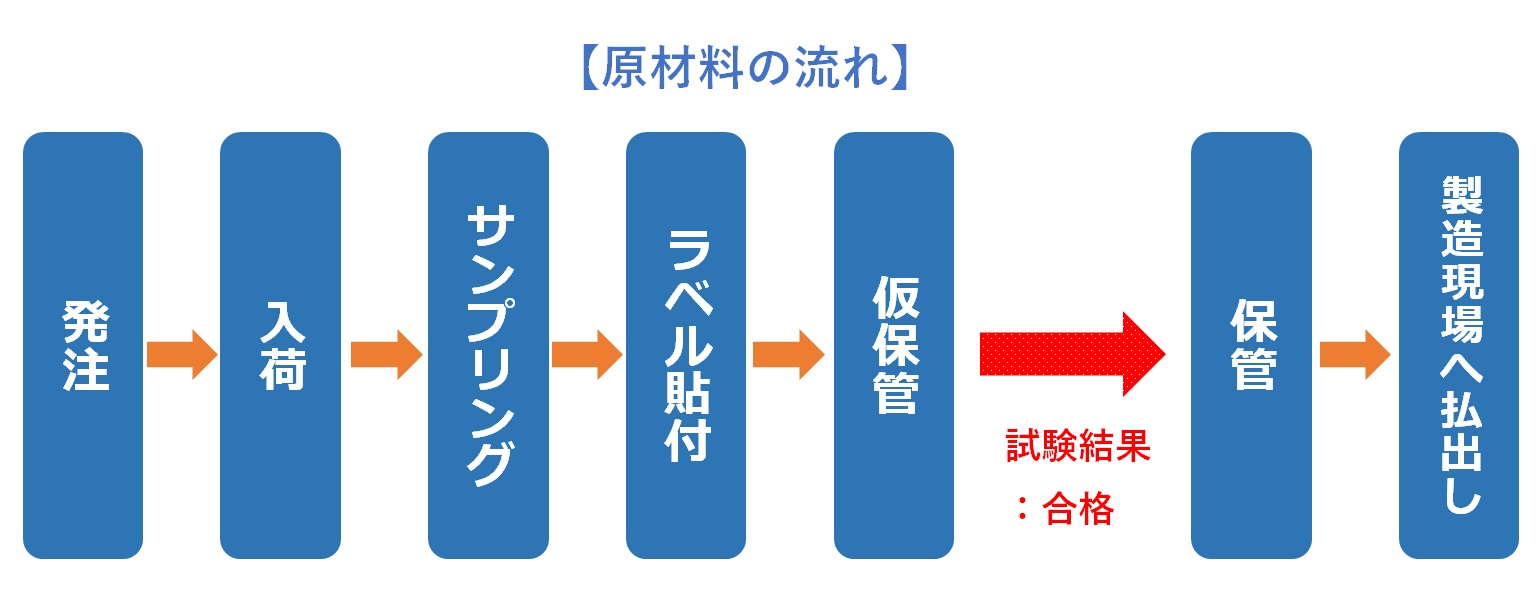
���i�����ɂ����āA���i���Ȑ��i�����肵�ċ������邽�߂ɂ́A���i�Ȍ��ޗ��Ǘ����s���ł���B�{�L���ł́A���ޗ��̔����������ꌟ���A��������ւ̕��o���Ɏ���܂ł̈�A�̗���ƁA�i����S�ۂ��邽�߂̏d�v�ȊǗ��|�C���g�ɂ��ĉ������B���ޗ��̗��ꌴ�ޗ��́A�uQA�i�i���ۏؕ��j�����F���������Ǝҁv�֔���...
�y�i���Ǘ��̒m���z�֘A���|�[�g
-
-
���ޗ��̃T���v�����O���ޗ�����ׂ����ہA������������{���邽�߁A�w�肳�ꂽ�e�킩��T���v���𒊏o�i�T���v�����O�j���Ȃ���Ȃ�Ȃ��B�T���v�����O�́A��������⎑�ޕ��傩��̈˗��Ɋ�Â��A�Ɨ������g�D�ł���QC�i�i���Ǘ����j�����{����̂������ł���B�������A��ƂɊ댯�⍢��i��Αтł̑Ή��A���ێ�����...
-
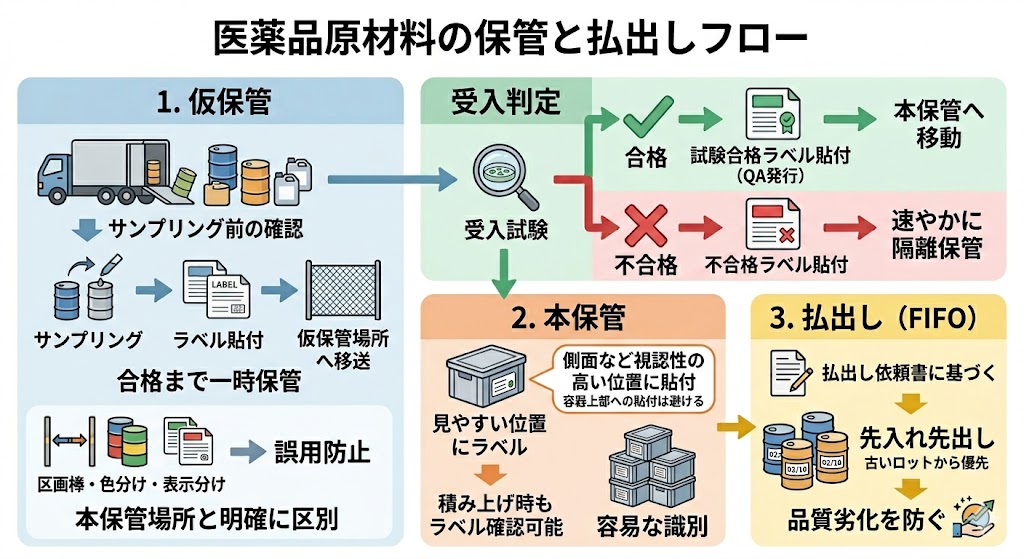
���ޗ��̉��ۊnj��ޗ��̃T���v�����O���{��́A�K�v�ȃ��x����\�t���A���₩�ɉ��ۊǏꏊ�ֈڑ����Ȃ���Ȃ�Ȃ��B���ۊǂƂ́A��������ɍ��i���A�����Ɏ������܂ł̈ꎞ�I�ȕۊǏ�Ԃ��w���B���̉��ۊǏꏊ�́A�{�ۊǏꏊ�Ɩ��m�ɋ�ʂ��Ȃ���Ȃ�Ȃ��B�ۊǂ��镔���A�I�A���邢�̓G���A���I�ɕ����邱...
-
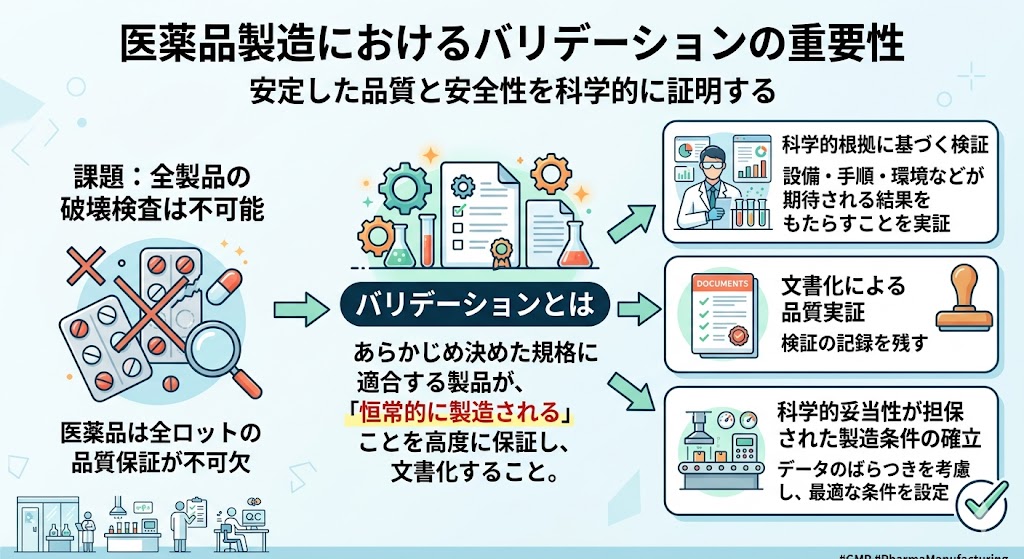
�o���f�[�V�����̒�`�Əd�v���������ꂽ��ЂƂ̈��i���A���ׂċK�i�ɓK�����A���S�ł���ƒf���ł���ł��낤���B���i�͂��̐�����A���ׂĂ̐��i���J�����Ĕj�����s���A�i�����m�F���邱�Ƃ͕s�\�ł���B�������A�����ɒ������鐻�i�ł���ȏ�A�S���b�g�̕i���ۏ͕s���ȐӖ��ł���B�����ŁA������...
-
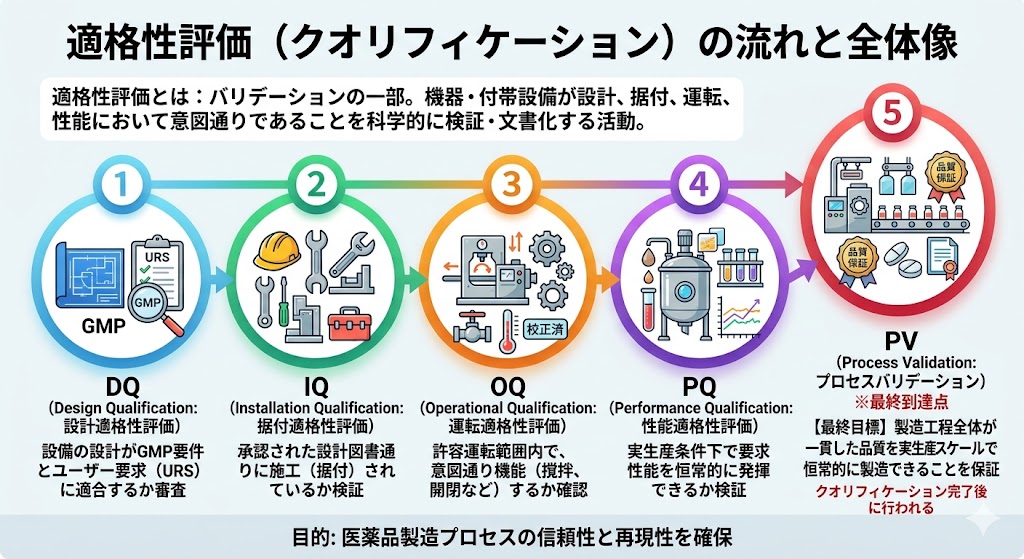
�N�I���t�B�P�[�V�����i�K�i���]���j�Ƃ́A�o���f�[�V�����̈ꕔ�ł���A�@���t�ѐݔ����K�ɐv�E�����t�����A�Ӑ}�����ʂ�ɉғ����A���҂���錋�ʂ��m���ɂ����炷���Ƃ��Ȋw�I�Ɍ����A�����������A�̊������w���B�@���ɁA�N�I���t�B�P�[�V�����̑S�̓I�ȗ���������B�@�@DQ�iDesign Qualifi...
-
-
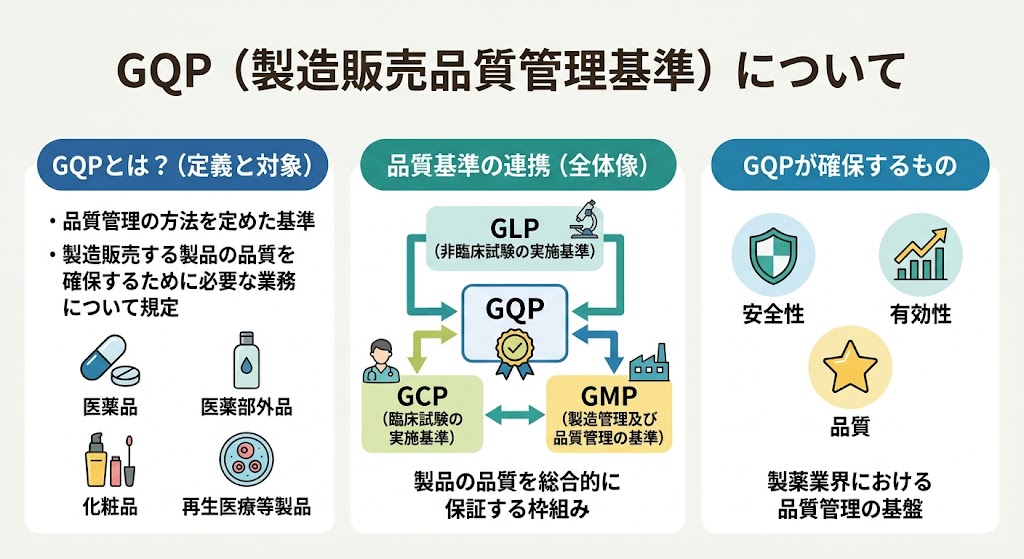
�����\�Z�N�����J���ȗߑ�S�O�\�Z�����i�A��O�i�A���ϕi�y�эĐ���Ó����i�̕i���Ǘ��̊�Ɋւ���ȗߖ@�i���a�O�\�ܔN�@����S�l�\�܍��j��\����̓��ꍆ�̋K��Ɋ�Â��A���i�A��O�i�A���ϕi�y�ш�Ë@��̕i���Ǘ��̊�Ɋւ���ȗ߂����̂悤�ɒ�߂�B�ڎ����́@����(�����E����)��...
-
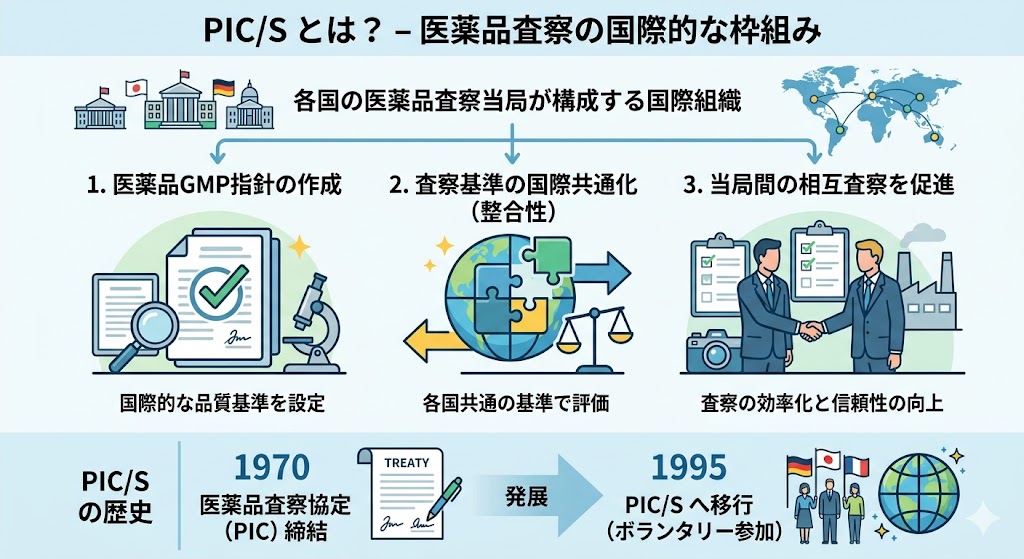
PIC/S�Ƃ́@PIC/S�iPharmaceutical Inspection Convention and Pharmaceutical Inspection Co-operation Scheme�j�Ƃ́A���i���@����y�ш��i���@�����X�L�[���̂��Ƃł���A�e���̈��i���@���ǂ���\������鍑��...
-
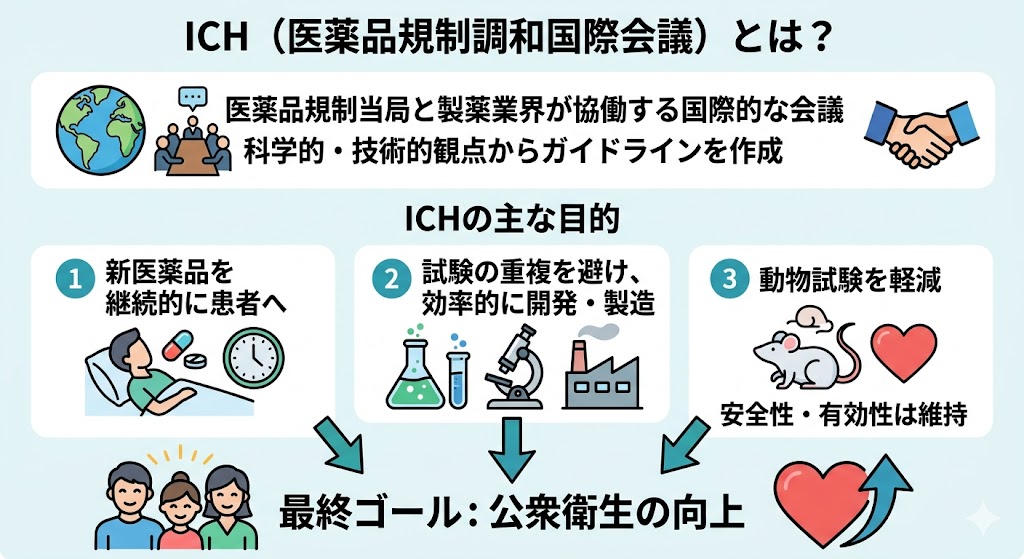
ICH�Ƃ�ICH�iInternational Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use�j�Ƃ́A���i�K�����a���ۉ�c�̂��Ƃł���BICH�́A�e�ɂ̈��i�K�����ǂƐ���ƊE...
-
�i���Ɋւ���K�C�h���C���uICH Q1�`Q14�v�Ƃ́@ICH�ł́AISO�̍l�������x�[�X�Ɉ��i�ƊE���L�̗v�f�������ꂽ�i���V�X�e���̃K�C�h���C�����쐬���A���\���Ă���B�@�i���Ɋւ���K�C�h���C���́AICH Q1����n�܂�A2026�N5�����݂ł�ICH Q1�`Q14�܂ō��肳��Ă���B ...
-
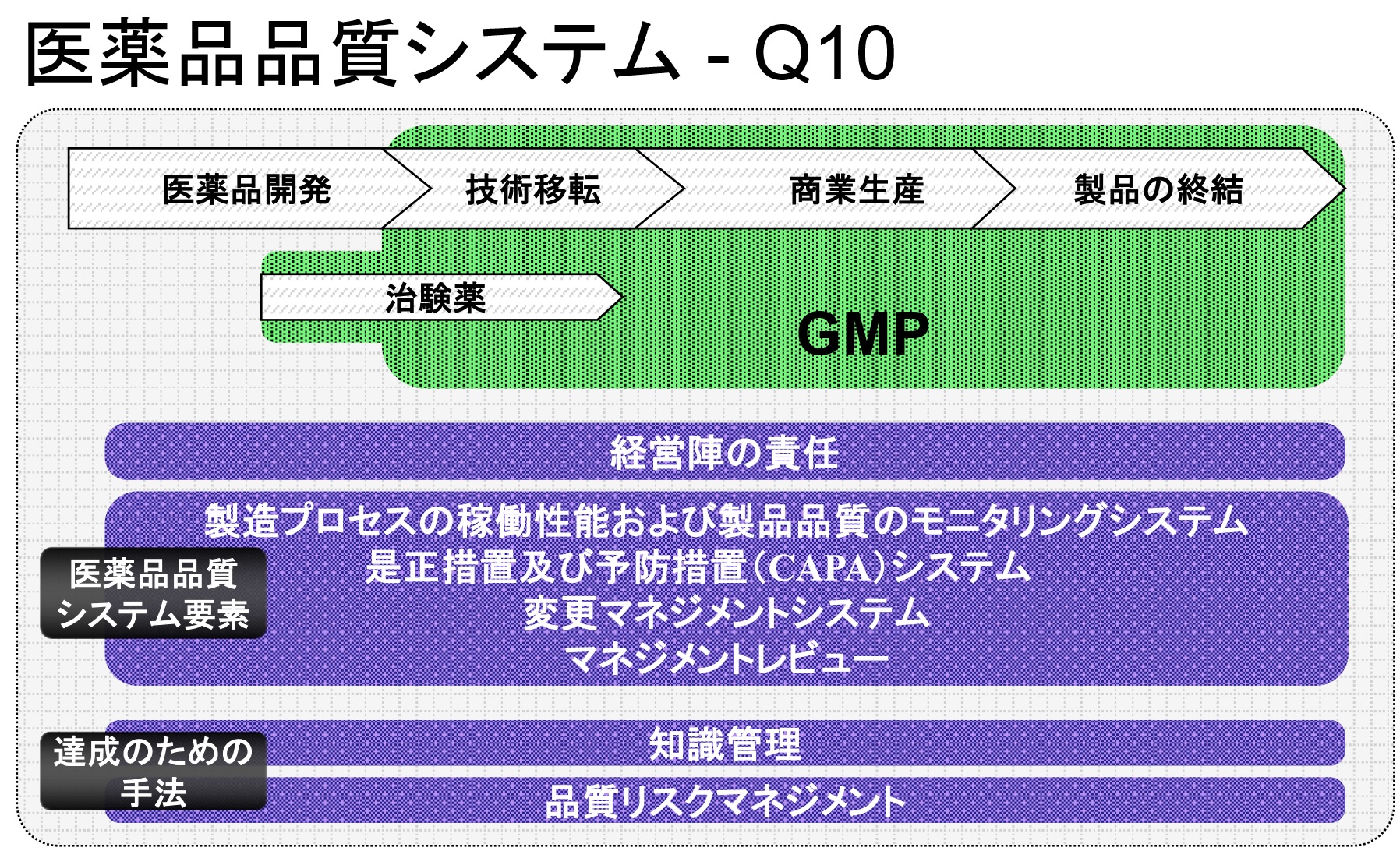
�uICH Q10�v�Ƃ́I�H�@ICH Q10�Ƃ́c���[�J�[�⌴�[�J�[�A�o�C�I���i�A�o�C�I�e�N�m���W�[��ΏۂƂ����A�uPQS�FPharmaceutical Quality System�i���i�i���V�X�e���j�v�ƌĂ��K�C�h���C���ł���B�@�@ICH Q10�i���i�i���V�X�e���j�́A�����Ƃ̂�...
- �g�b�v�y�[�W
- �i���Ǘ��̒m��