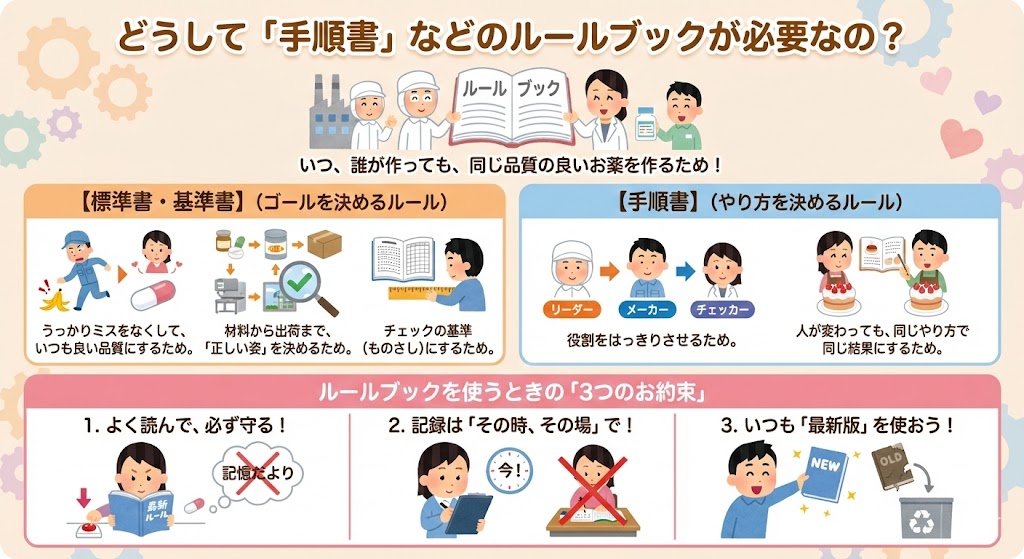
GMP遵守の鉄則:製造担当者が越えるべき「5つの壁」
〜ヒューマンエラーを防ぎ、医薬品の品質を守る実践〜
「手順通りにやったつもりだった」「忙しくて記録を後回しにした」。
医薬品製造の現場で起こるGMP違反の多くは、悪意ではなく、こうした人間の心理や油断(ヒューマンエラー)から生まれます。作業者がGMPを確実に守るために、日々の業務で意識すべき「5つの壁」とその乗り越え方を解説します。

製造しているものは単なる「モノ」ではなく、誰かの命を救うための「医薬品」である。
製造担当者に最も求められるのは、GMPの知識以前に「自分の大切な家族に、自信を持ってこの薬を飲ませることができるか」と常に自問する姿勢である。
この想像力こそが、GMP遵守の最後の砦となる。
作業の一つひとつが患者の生命に直結していることを自覚し、主体的かつ積極的に業務に関与しなければならない。
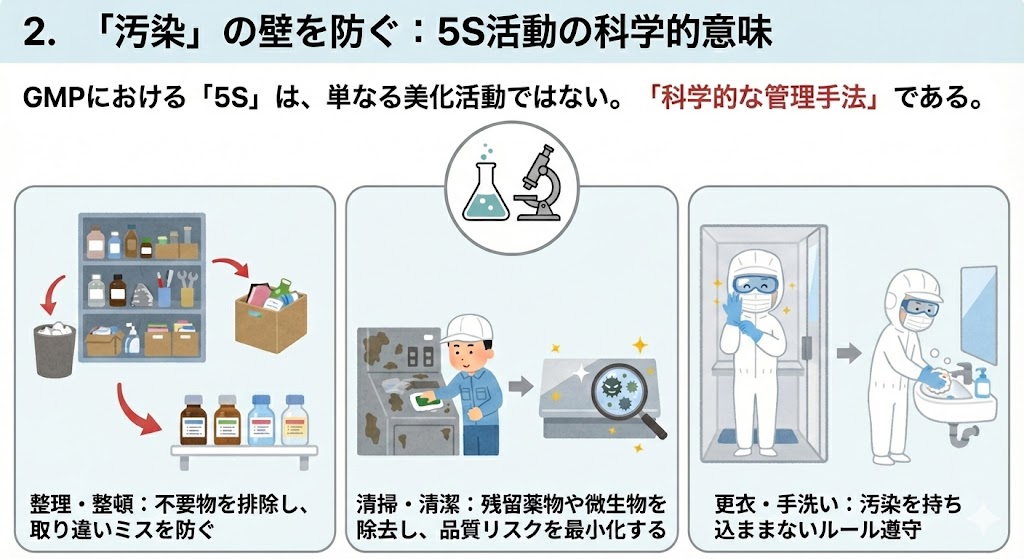
GMPにおける「5S(整理・整頓・清潔・清掃・躾)」は、単なる美化活動ではない。
交叉汚染(クロスコンタミネーション)や異物混入を防ぐための「科学的な管理手法」である。
製造担当者は、以下の目的を理解し、衛生管理を徹底することが求められる。
・整理・整頓:不要物を排除し、取り違いミス(Mix-up)を物理的に防ぐ。
・清掃・清潔:残留薬物や微生物を除去し、品質リスクを最小化する。
定められた更衣手順や手洗いは、汚染を持ち込まないための必須要件である。一挙手一投足、ルールを遵守せねばならない。
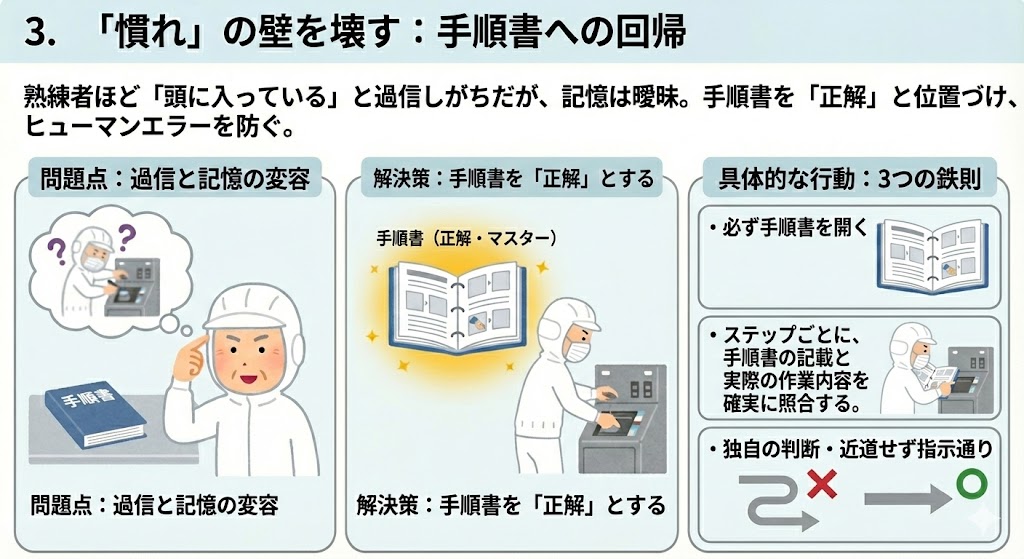
熟練者になるほど、「頭に入っている」と過信し、手順書を見ずに作業しがちである。しかし、人間の記憶は曖昧になり、都合よく変容するものである。
思い込みによるミス(ヒューマンエラー)を防ぐため、常に目の前の手順書を「正解(マスター)」と位置づける必要がある。
・「知っている作業」であっても必ず手順書を開く。
・ステップごとに、手順書の記載と実際の作業内容を確実に照合する。
・独自の判断や近道をせず、指示通りに実行する。

「数値を修正して規格内に入れたい」「多忙ゆえにまとめて記録したい」。こうした誘惑は、企業の信頼を一瞬で崩壊させる。
製造担当者には、記録をALCOA+の原則に従い、誠実に行う高い倫理観が不可欠である。
記録とは「品質を証明する証拠」である。実行した事実をありのままに、その場で記録すること。
【禁止事項】
・バックデート(過去の日付での記録捏造)
・データの書き換え・改ざん
・メモ書きの転記や、事実に基づかない数字の作成

「叱責されたくない」という心理が、小さな逸脱を隠蔽させ、やがて重大な健康被害へと拡大させる。
GMP遵守組織に必要なのは、「悪い知らせほど早く報告する」文化である。
異常や逸脱を発見した際の報告は、非難されるべきことではなく、品質を守ったファインプレーとして評価されるべき行動である。
躊躇なく「報告・連絡・相談」を行い、チーム全体で品質リスクの解決にあたることが義務である。
まとめ
医薬品製造に携わるすべての従業員は、単に規則を守るだけでなく、品質の守り手としてGMP実施に主体的に関与する。
また、GMPの原則や要件を正しく理解し、それらを実践するための教育訓練を継続的に受けることが不可欠である。
自分の担当する業務や責任の範囲を明確に自覚し、手順書を読み込んで理解し、プロフェッショナルとしての技術を磨き続ける必要がある。