ロット記録書の照査と承認
ロット記録書の照査と承認
製造記録書、試験管理記録書、包装記録書、ラベル記録書など、当該ロットの製造および試験に関係するすべての記録を総称して「ロット記録書」と呼ぶ。
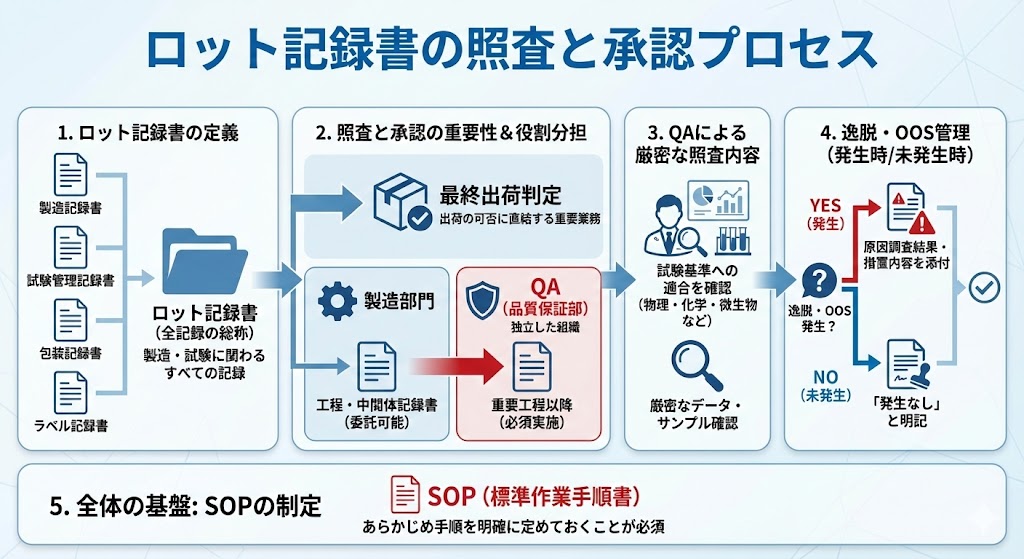
ロット記録書の照査および承認は、製品の最終的な出荷判定に直結するため、極めて重要な業務である。
工程記録書や中間体の製造記録書に関する照査は、製造部門へ委託できる場合がある。しかし、重要工程以降の記録書の照査は、独立した組織であるQA(品質保証部)が実施しなければならない。
QAによる照査では、ロット記録書に含まれるデータやサンプルが、品質管理部門の規定した各種試験(物理的試験、化学分析、微生物学的検査など)の判定基準に適合しているかを厳密に確認する。
製造工程において逸脱やOOS(Out of Specification:規格外試験結果)が発生した場合には、その原因調査結果および措置内容をロット記録書に添付する。仮にこれらが発生しなかった場合であっても、「逸脱およびOOSの発生なし」と明記することが求められる。
これら照査および承認の実施方法は、あらかじめSOP(標準作業手順書)を制定し、その手順を明確に定めておく必要がある。
照査とは、記録書の「内容の正しさ」を客観的証拠に基づき確認することである。一方、承認とは、記録書「内容の正当性」を責任をもって認めることである。
それぞれの具体的な実施内容を以下に示す。
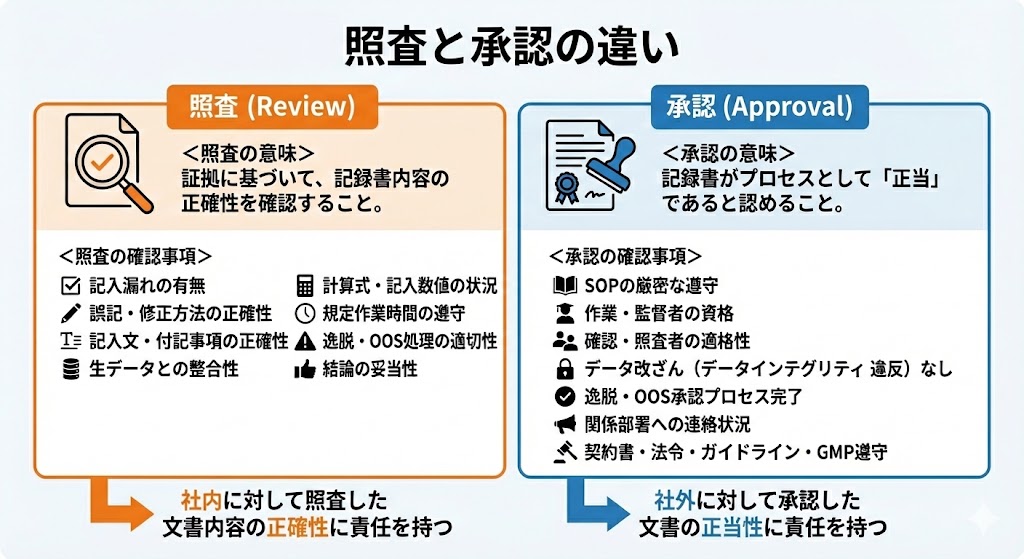
<照査の意味>
証拠に基づいて、記録書内容の正確性を確認すること。
<照査の確認事項>
・記入漏れの有無の確認
・誤記および修正方法の正確性確認
・記入文、付記事項の正確性確認
・生データとの整合性調査
・計算式および記入数値の状況確認
・規定された作業時間の遵守確認
・逸脱およびOOS処理の適切な実施確認
・結論の妥当性確認
<承認の意味>
記録書がプロセスとして「正当」であると認めること。
<承認の確認事項>
・SOPが厳密に遵守されているかの確認
・作業者および監督者の教育訓練・資格の確認
・確認者および照査者の適格性確認
・データ改ざん(データインテグリティ違反)がないことの確認
・逸脱、OOSの承認プロセス完了の確認
・関係部署への連絡状況の確認
・契約書、各種法令、ガイドライン、およびGMP省令の遵守確認
総じて、照査者は「社内に対して照査した文書内容の正確性に責任」を持ち、承認者は「社外に対して承認した文書の正当性に責任」を持つと言い換えることができる。
【用語解説】
| ロット記録書 | 当該ロットの製造および試験に関係するすべての記録(製造記録書、試験管理記録書、包装記録書など)をまとめた文書。 |
|---|---|
| QA(品質保証部) | Quality Assuranceの略。 製品が規定された品質要件を満たしていることを保証し、製造部門から独立して照査・承認などの業務を担う部門。 |
| 逸脱 | 製造工程や品質試験において、あらかじめ定められた基準、規格、またはSOPなどの手順から外れる事象が発生すること。 |
| OOS | Out of Specificationの略。 試験において、得られた結果が規定の規格値や判定基準から外れている状態(規格外試験結果)。 |
| SOP | Standard Operating Procedureの略。 作業の均質性と品質を保つため、作業手順や留意点などを詳細に定めた標準作業手順書。 |
| 生データ | 観察や測定などによって得られた最初の記録(ローデータ)。 照査において、記録書の数値が正しいことを客観的に裏付ける根拠となる。 |
| データインテグリティ | データの完全性、正確性、一貫性を保証すること。 データの改ざんや消失がない状態を維持し、記録の信頼性を担保するGMP上の重要概念。 |
| GMP | Good Manufacturing Practiceの略。 医薬品の製造管理および品質管理の基準であり、製品の品質と安全性を確保するための厳格なルール。 |


