CIPとSIPとは!?
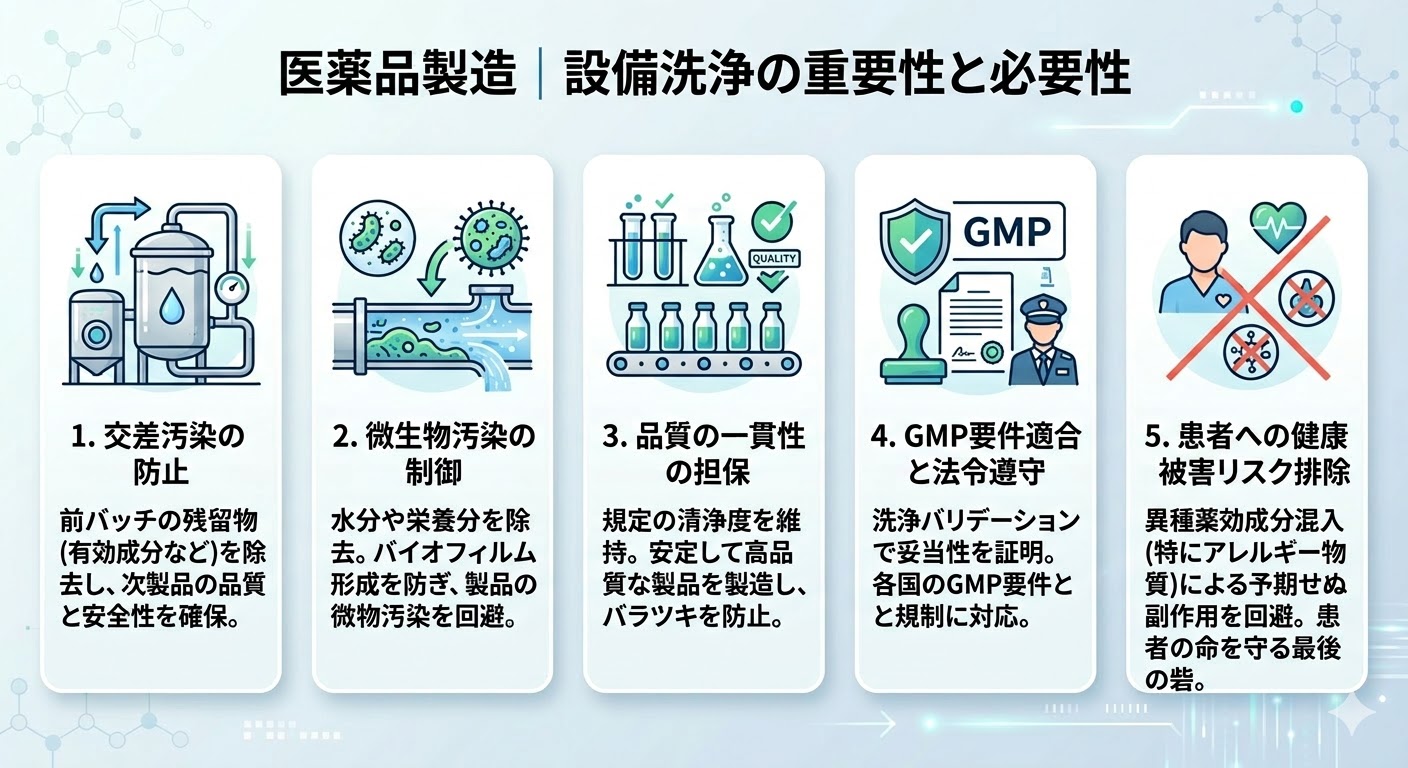
医薬品の製造設備は、異物の混入やクロスコンタミネーション(前バッチの成分混入)を防ぎ、常に高度な清浄度を保つ必要がある。
各バッチの製造終了後は、使用した機器を十分に洗浄し、必要に応じて消毒や滅菌を実施しなければならない。
生産設備を分解・移動することなく、定置状態のまま自動的に洗浄するシステムをCIP(Cleaning in Place:定置洗浄)、同様に定置状態のまま滅菌するシステムをSIP(Sterilization in Place:定置滅菌)と呼ぶ。
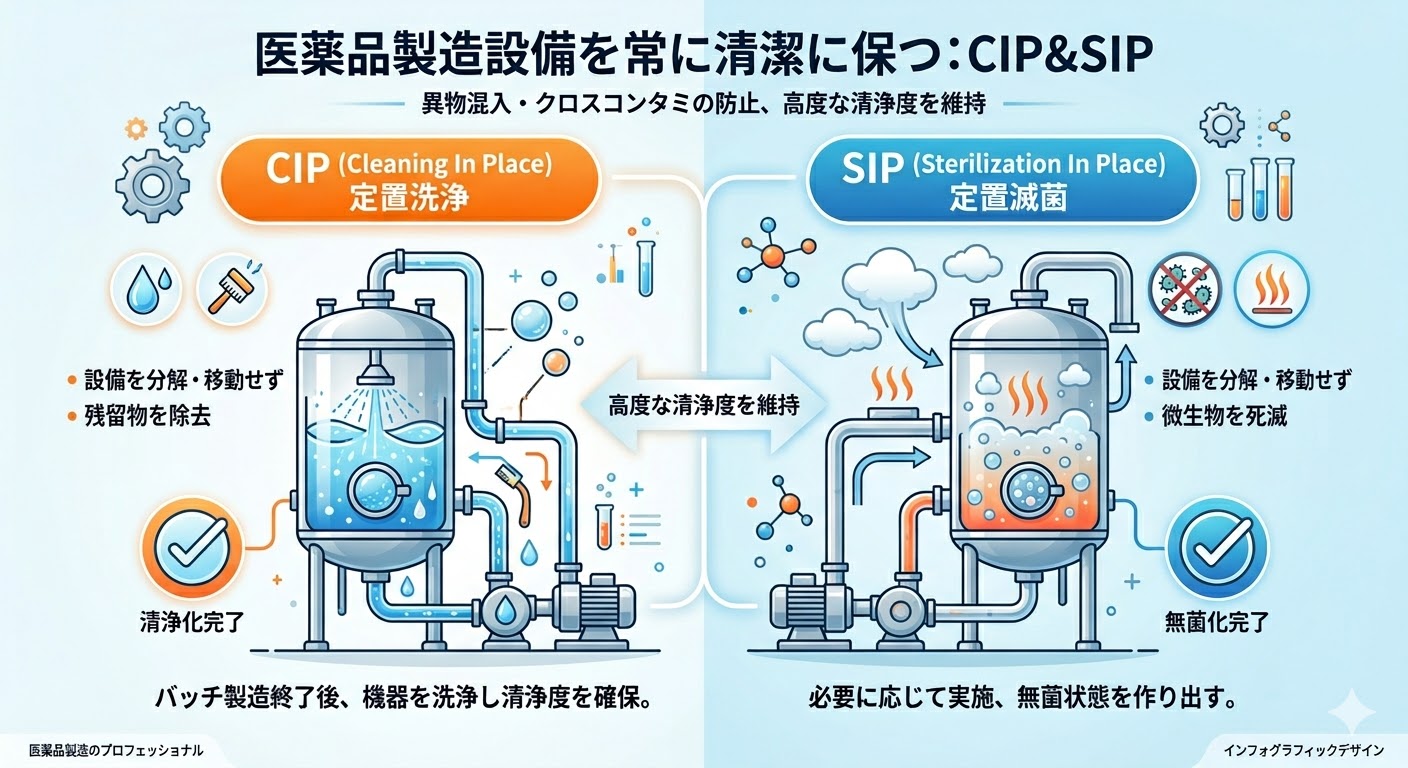
CIPは、設備内部や配管網を分解せずに洗浄するプロセスである。
医薬品製造において、製品の残留物や微生物による汚染を防ぐため、機器や配管は定期的かつ確実に洗浄されなければならない。
CIPシステムでは、精製水や専用の洗浄液(酸、アルカリ、界面活性剤など)を用いて汚れを物理的・化学的に除去する。
タンク内部はスプレーボールからのシャワー洗浄、撹拌翼などの複雑な構造物は貯め洗い、配管内部は乱流域に達する一定以上の流速(一般的に1.5m/s以上)を保つことで、確実な洗浄効果を担保する。
一般的なCIPサイクルは、予備洗浄、洗浄液による循環洗浄、そして清浄な水による最終リンスで構成される。特に注射剤の製造ラインでは、最終リンス水にWFI(注射用水)を使用することが義務付けられている。また、CIP設備自体は、洗浄液を貯留するタンク、送液ポンプ、および洗浄液を適切な温度に昇温するための熱交換器などで構成される。
CIPの適切な運用により、設備や配管内の残留物および微生物を再現性よく効果的に除去し、製造プロセスの安全性と製品品質を確保する。
SIPは、洗浄後の設備、タンク、配管等の系内を定置状態のまま滅菌するプロセスである。
無菌製剤の製造など、微生物汚染リスクを極限まで排除すべき工程においては、製造プロセスを開始する前に設備全体を完全に滅菌する必要がある。
SIPでは、一般的に精製水やWFIを原水として生成されたクリーンな飽和水蒸気(ピュアスチーム)を生産設備の系内に導入する。系内全体を規定の滅菌温度まで昇温し、すべての微生物を死滅させて無菌状態を達成する。
これにより、微生物汚染のリスクを最小限に抑え、無菌製品の安全性と品質を保証する。
系内を昇温し、規定温度を一定時間保持(例:121℃で20分間以上)する際、配管内の空気溜まり(エアバインディング)やドレン(凝縮水)の滞留があると、スチームが隅々まで行き届かず、温度低下による滅菌不良箇所(コールドスポット)が生じる。したがって、機器や配管のサニタリー設計(適切な配管勾配やスチームトラップの配置)およびSIP時の制御には、緻密な設計と検証が要求される。
ピュアスチーム発生器(Pure Steam Generator)は、医薬品製造に不可欠な高品質のクリーン蒸気を生成する装置である。
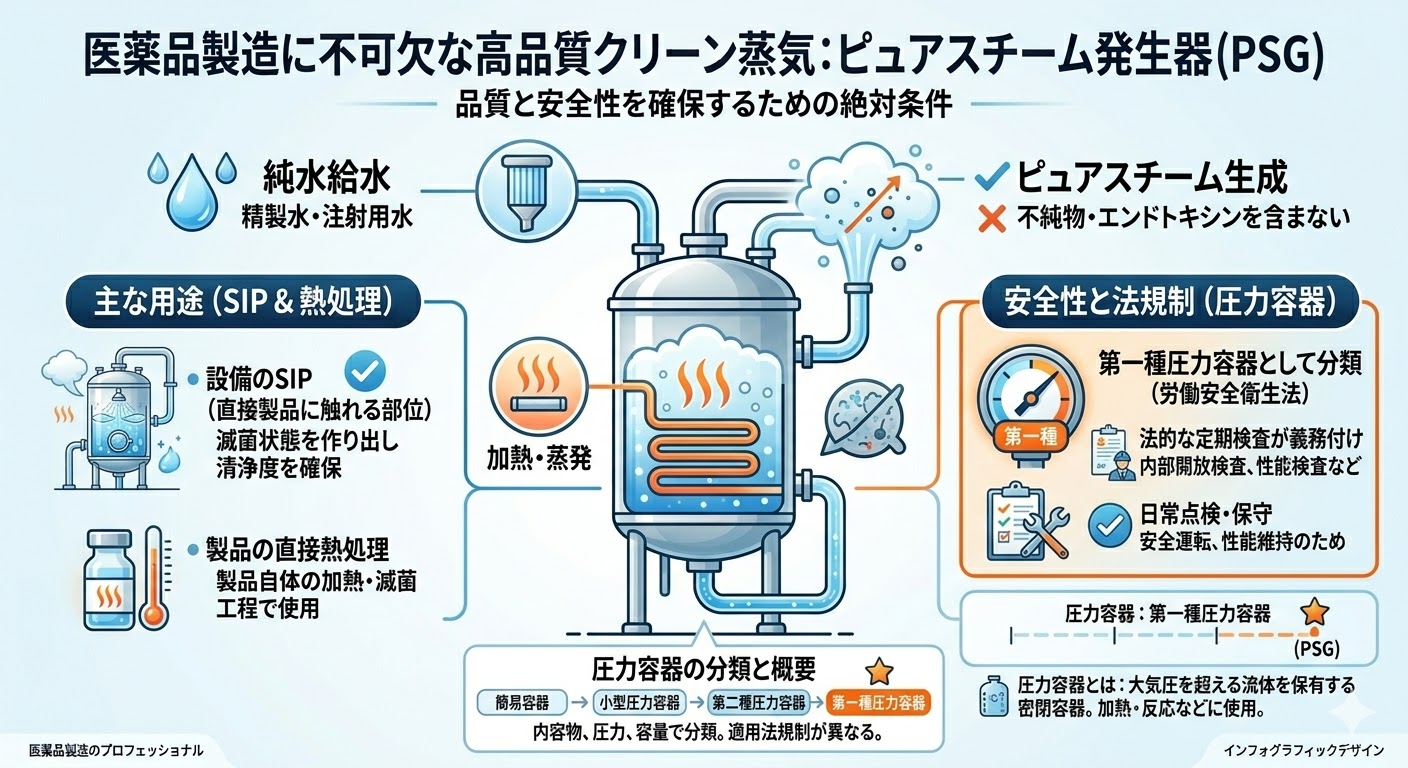
純水(精製水や注射用水)を給水として加熱・蒸発させ、不純物やエンドトキシンを含まないピュアスチームを生成する。この高品質な蒸気は、直接製品に触れる可能性のある設備のSIPや、製品の直接熱処理において、品質と安全性を確保するための絶対条件となる。
SIPに不可欠なピュアスチーム発生器は、高圧の蒸気を扱うため、労働安全衛生法において一般的に「第一種圧力容器」に分類される。
蒸気の品質と設備の安全性を維持するため、日常の点検・保守に加え、法的な定期検査が義務付けられている。
圧力容器とは、内部に大気圧を超える気体または液体を保有し、内容物の加熱・反応工程を行ったり、高温・高圧の流体を蓄積したりする密閉容器を指す。
これらは内容物や圧力・容量の規模に応じて、第一種圧力容器、第二種圧力容器、小型圧力容器、または簡易容器などに分類され、それぞれに適用される法規制が異なる。
第一種圧力容器は、爆発等の事故による危険性が高いため、製造許可から輸入、設置の各段階において都道府県労働局(または労働基準監督署長)等による厳格な検査が義務付けられている。さらに、使用開始後も登録性能検査機関による年1回の「性能検査」を受審し、合格しなければ使用を継続することができない。
また、事業者は第一種圧力容器の取り扱いに際し、容器の種類や規模に応じて定められた国家資格を有する者の中から「第一種圧力容器取扱作業主任者」を選任し、作業の直接指揮や設備の安全管理を行わせる義務がある。
関連する法規制や資格の詳細については、日本ボイラ協会ホームページ等で最新の情報を確認することが推奨される。
【用語解説】
| CIP(定置洗浄) | Cleaning in Placeの略。設備や配管を分解することなく、内部に洗浄液やリンス水を循環させて洗浄する。クロスコンタミネーションを防止する。 |
|---|---|
| SIP(定置滅菌) | Sterilization in Placeの略。CIP完了後の設備内にピュアスチーム等を導入し、分解せずに定置状態のまま系内全体を無菌化(滅菌)する。 |
| WFI(注射用水) | Water for Injectionの略。精製水をさらに蒸留・ろ過し、エンドトキシンや微生物を厳密に排除した超純水。注射剤の調製や、重要設備の最終リンスに使用される。 |
| ピュアスチーム | 精製水やWFIを原水として発生させた、不純物やエンドトキシンを含まない清浄な飽和水蒸気。クリーン・スチームとも呼ばれ、SIPに不可欠である。 |
| 第一種圧力容器 | 大気圧を超える圧力の気体や液体を内部に保有する容器のうち、労働安全衛生法で定められた一定の規模・基準を超えるもの。厳格な製造基準と年1回の性能検査が義務付けられている。 |