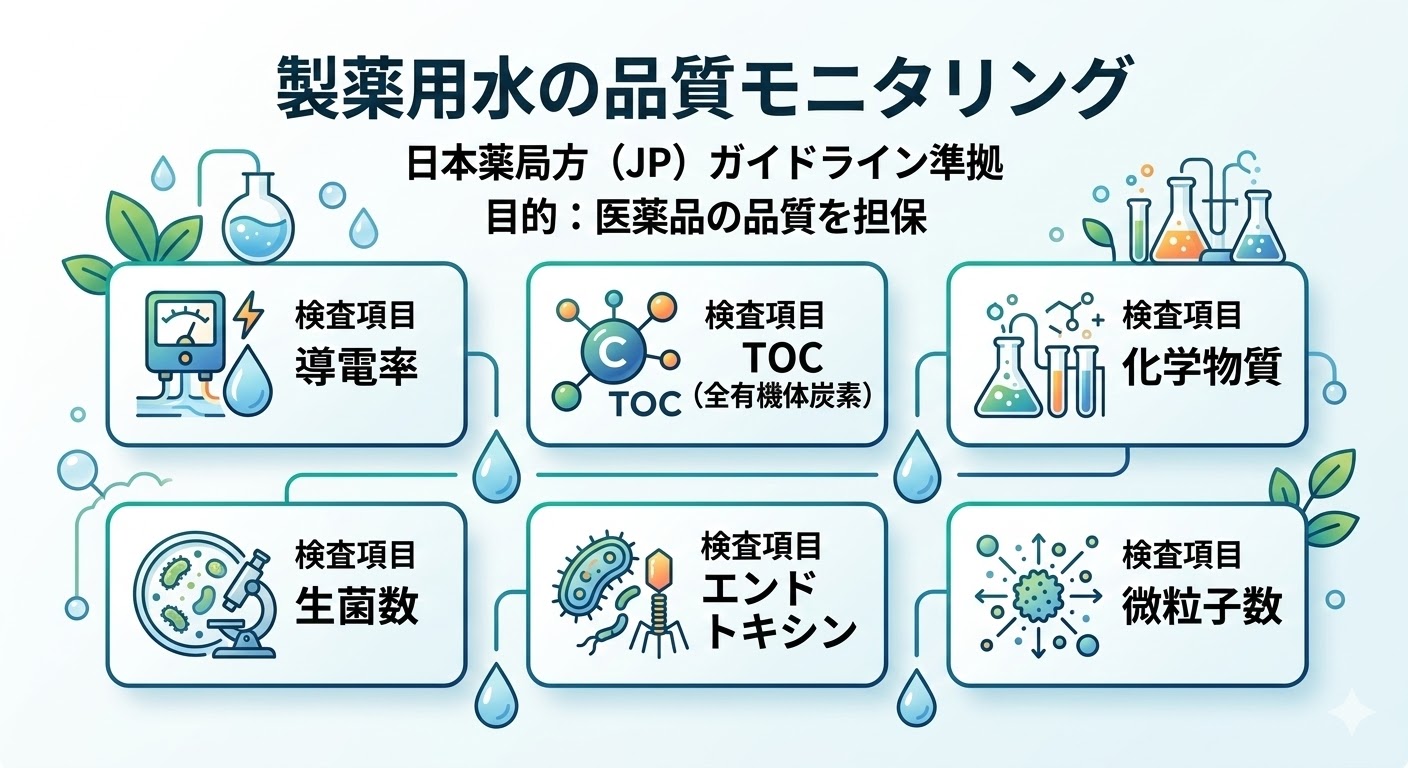
製薬用水を製造する設備
製薬用水設備は、原水に含まれる不純物を取り除き、規格に合致する水準を確保するための一連の装置群(トータルシステム)である。そのため、原水の水質や各装置の処理能力によって最適な設備構成が変化する。
設計に際しては、季節変動を含めた詳細な水質データを事前に把握することが極めて重要となる。以下に、一般的な製薬用水の製造プロセスを示す。
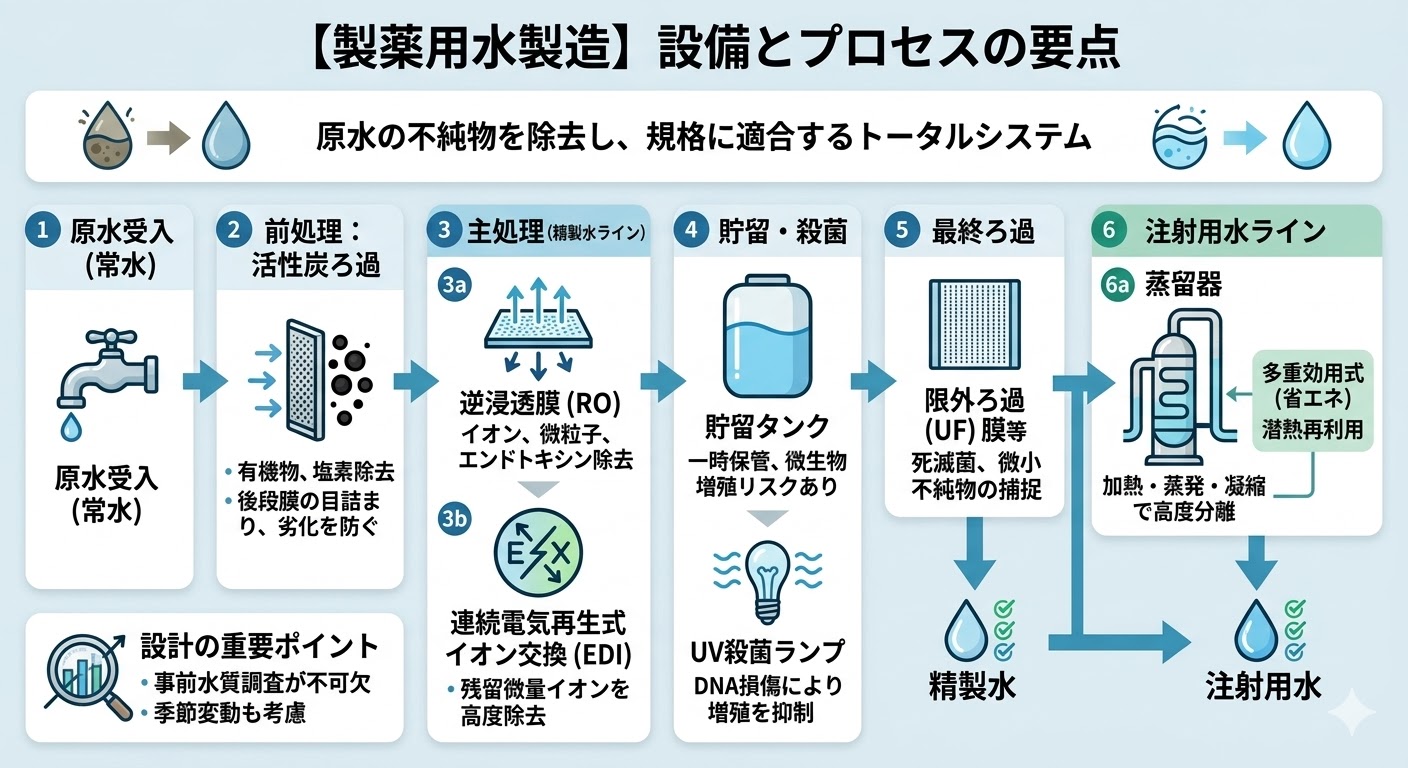
まず前処理として、「常水」の基準を満たす原水に対し活性炭ろ過を行う。これは、後段の逆浸透(RO)膜に付着してファウリング(汚染・目詰まり)を引き起こす有機物や、RO膜を劣化させる遊離残留塩素を除去するためである。
続いて、逆浸透(Reverse Osmosis: RO)膜によって水中のイオン、微粒子、エンドトキシン(パイロジェン)の大半を除去する。さらに連続電気再生式イオン交換器(Electric De-Ionization: EDI)を通水し、残留する微量なイオンを高度に除去する。
純水製造ラインの精製速度には限界があるため、製造された純水は一時的に貯留タンクへ保管される。しかし、塩素を持たない純水はタンク内で微生物が増殖するリスクを伴う。
その対策として、UV(短波長紫外線)ランプによる殺菌が行われる。波長254nmの短波長紫外線は微生物のDNAを損傷させ、その増殖能力を抑制する働きがある。
死滅した菌体等の微小な不純物は、採水ラインに設置された中空糸フィルター(限外ろ過(Ultrafiltration: UF)膜など)によって最終的に捕捉・除去され、品質基準を満たした「精製水」となる。
「注射用水」の製造には、精製水よりもさらに厳格な微生物管理とエンドトキシンの除去が要求される。そのため、精製水を蒸留器で加熱・気化させ、その蒸気を冷却・凝縮させる蒸留法を用いてエンドトキシンを分離し、「注射用水」を製造する。
蒸留器は供給水を蒸発缶で気化させ、コンデンサーで凝縮する構造を持つ。複数の蒸発缶を直列に接続した多重効用式蒸留器は、前段の蒸発潜熱を次段の加熱源として再利用できるため、省エネルギー対策として有効である。
「精製水」および「注射用水」のユースポイント(使用箇所)は工場内に多数存在し、その消費量は時間帯によって大きく変動する。ピーク時の最大使用量に合わせて装置を選定するのは非効率であるため、製薬用水は適切な容量のタンクに貯留され、そこから各ユースポイントへ供給される。
不純物を取り除いた製薬用水は、残留塩素を含む水道水と比較して微生物が極めて繁殖しやすく、水質劣化が早い。したがって、供給設備には微生物の増殖を抑制し、水質を維持するための工夫が施されている。
まず、水が滞留する箇所は微生物増殖の温床となるため、供給水は常時循環させる。タンク内においても、気液境界面や上面にスプレーボールを設置して常時水流を当てる。また、計器類のセンサー座や配管の分岐部など、水流が滞る構造をデッドレッグと呼び、これらが常に乱流によって洗浄されるよう配管設計を行う。
さらに、より厳格な微生物管理が要求される「注射用水」では、ループ内の水を常時高温(80℃以上)で循環させ、各ユースポイントで個別に使用温度まで冷却して供給する方式が一般的である。
製薬用水の供給システムは、定期的な殺菌または滅菌(熱交換器を用いた熱水殺菌や、純蒸気の供給など)が可能な構造とし、系内のバイオバーデン(材料や製品上に存在する生育可能な微生物の集団)を継続的に低減させることが重要である。
システム内に一度バイオフィルムと呼ばれる強固な微生物の集合体が形成されると、滅菌操作を行っても数日で再び微生物が繁殖し、生菌数の基準を満たすことが困難になる。
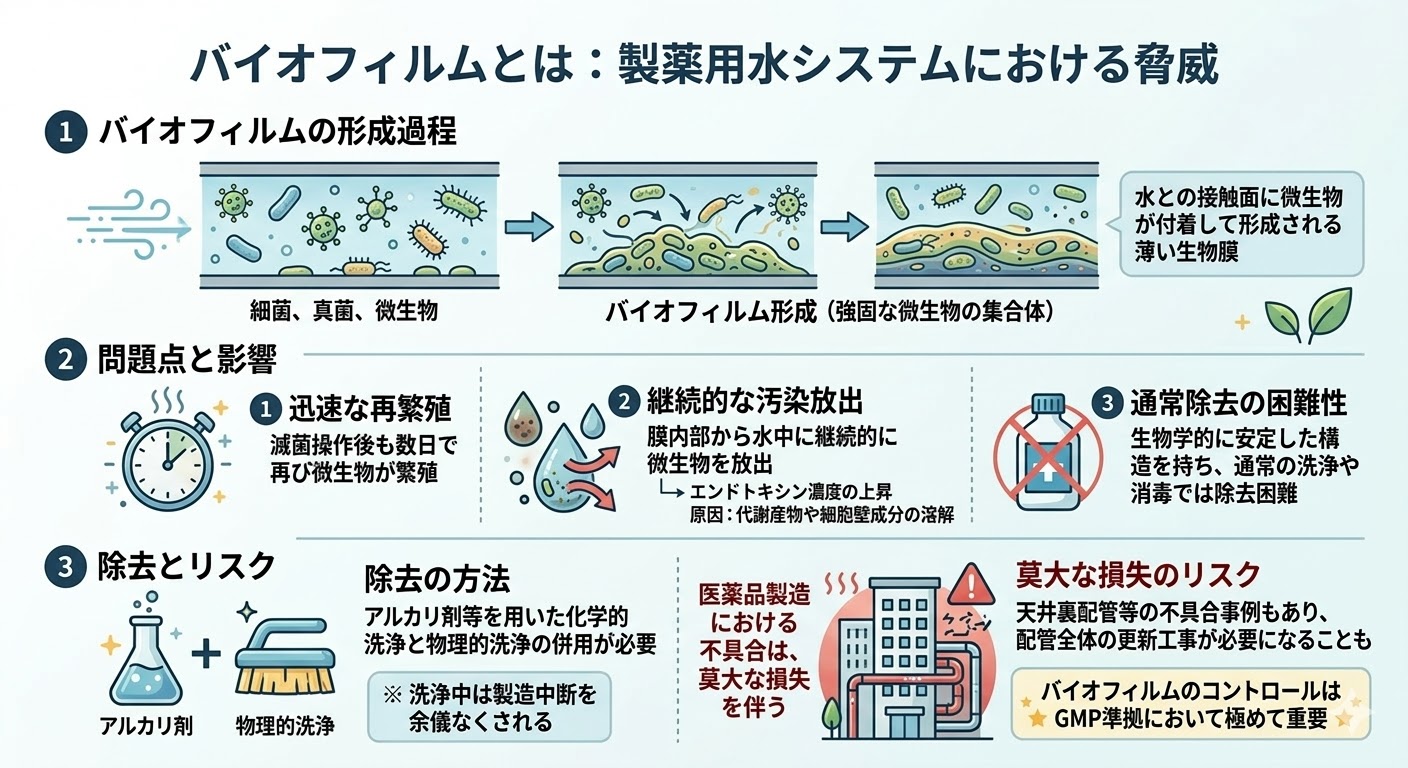
バイオフィルムとは、細菌や真菌などの微生物が水との接触面に付着して形成される薄い生物膜である。
バイオフィルムが形成されると、膜内部から水中に継続的に微生物が放出され、製薬用水の品質に悪影響を及ぼす。
さらに、微生物の代謝産物や細胞壁成分が溶解することで、エンドトキシン濃度を上昇させる原因にもなる。
この生物膜は生物学的に安定した構造を持つため、通常の洗浄や消毒では除去が極めて難しい。
除去するためには、アルカリ剤等を用いた化学的洗浄と物理的な洗浄を併用する必要があるが、洗浄中は製薬用水が使用できず、製品の製造を中断することになる。
最悪の場合、天井裏などの隠蔽配管にバイオフィルムが形成され、配管全体の更新工事を余儀なくされた事例も存在する。
医薬品製造における製薬用水設備の不具合は、莫大な損失を伴う。
バイオフィルムのコントロールは、GMPや製薬業界の規制要件に準拠する上で極めて重要である。
製薬用水設備も生産設備と同様に、厳格なバリデーションを実施する。
製薬用水設備のバリデーションは、設備メーカーの設計仕様がユーザー要求およびGMPに適合しているかを検証するDQ(設計適格性評価)から始まり、その後装置が製作される。
工場への搬入および据付工事後、配管や電気工事等の状態を確認するIQ(据付適格性評価)を実施する。
続いて、実際の造水を通じて各種パラメーターをチューニングし、自動運転の検証、造水能力、熱水循環温度、滅菌機能などを確認するOQ(運転適格性評価)を行い、ユーザーに引き渡される。
受領したユーザー側では、運転管理プログラムを検討しつつ、GMPソフトを含めた運用・水質管理手法の妥当性を評価するPQ(稼働性能適格性評価)を実施する。
新工場を建設する場合、生産設備の立ち上げには製薬用水が不可欠である。そのため、プロジェクト全体のスケジュールを考慮し、早い段階で製薬用水設備を立ち上げる必要がある。
製薬用水設備が稼働し、規格に適合する水質が確保された後は、恒常的に水質を維持するための管理方法を確立しなければならない。
製薬用水は劣化しやすいため、定期的な滅菌・殺菌により系内を清浄に保つとともに、要求水質が継続的に満たされていることを監視(モニタリング)する水質管理プログラムが不可欠である。
バリデーションにおいては、水質を維持するための適切な殺菌頻度や、サンプリング箇所・方法などのモニタリング計画の妥当性を証明できるデータを取得しておく必要がある。
【用語解説】
| RO(逆浸透)膜 | 水を通し、イオンや微粒子、微生物などの不純物を透過させない半透膜。 Reverse Osmosisの略。 |
|---|---|
| EDI(連続電気再生式イオン交換器) | イオン交換樹脂とイオン交換膜、直流電流を組み合わせ、水中の微量イオンを連続的に除去する装置。 Electric De-Ionizationの略。 |
| UF(限外ろ過)膜 | 微細な孔を持つろ過膜。主に微生物やエンドトキシン(パイロジェン)、微粒子の除去に用いられる。 Ultrafiltrationの略。 |
| デッドレッグ | 配管の分岐部などで水流が滞留しやすい行き止まり構造のこと。 微生物の温床となるため設計段階での排除が求められる。 |
| バイオフィルム | 微生物が配管内壁などに付着し、自ら分泌する粘液状の物質で覆われて形成される強固な生物膜。 |
| バリデーション | 設備の設計や手順が、期待される結果(要求品質)を恒常的に与えることを科学的根拠に基づいて検証し、文書化する活動。 |