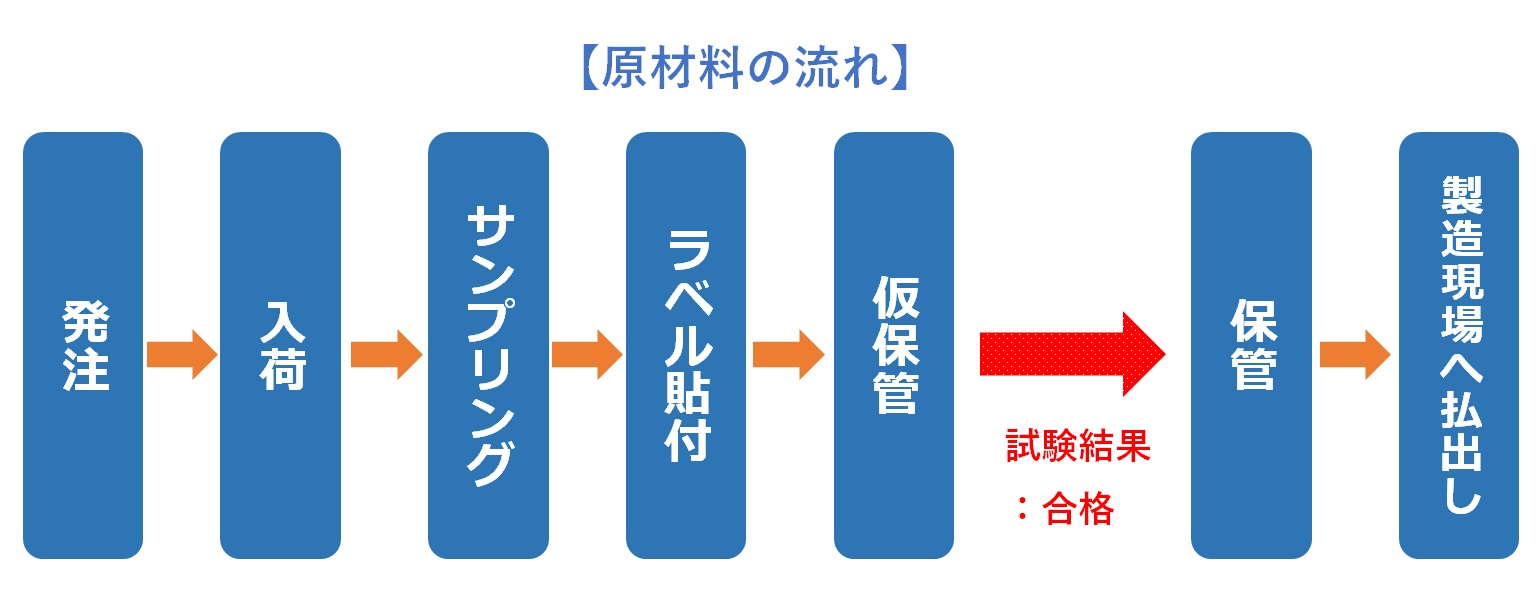
原材料の流れ「発注と受入れ検査」
医薬品製造において、高品質な製品を安定して供給するためには、厳格な原材料管理が不可欠である。
本記事では、原材料の発注から受入れ検査、製造現場への払出しに至るまでの一連の流れと、品質を担保するための重要な管理ポイントについて解説する。
原材料は、「QA(品質保証部)が承認した供給業者」へ発注する。
原材料が医薬品製造工場へ到着した後、入荷、サンプリング、ラベル貼付、仮保管、製造現場への払出しという一連の工程を進める。
これらの工程には、それぞれ個別のSOP(標準作業手順書)を作成する。発注から払出しまでを単一のSOPに集約するよりも、工程ごとに分割して作成する方が望ましい。
これは、各工程において時間的・場所的な差異が存在し、担当者も異なるケースが多いためである。
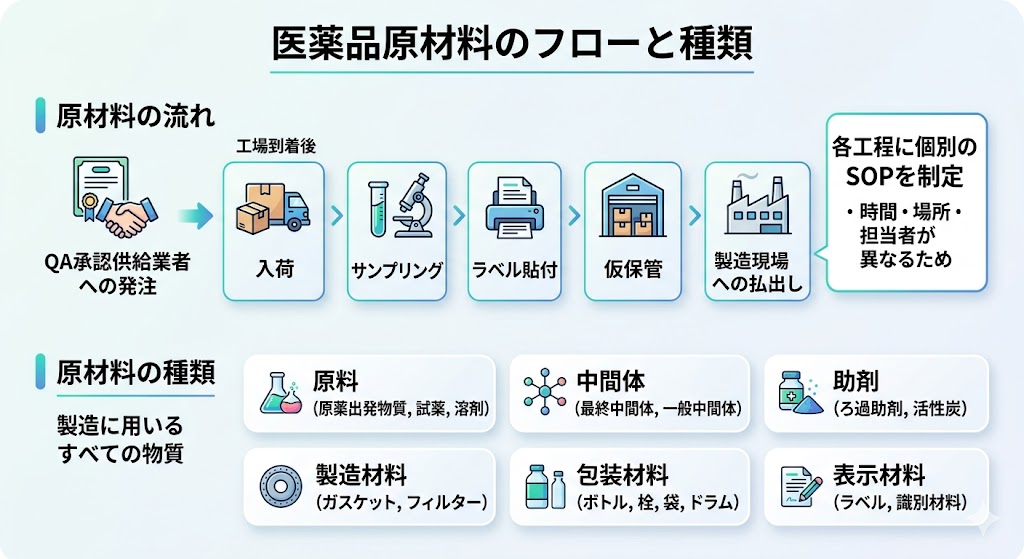
医薬品製造において、製品製造に用いるすべての物質は原材料と呼ばれ、主に以下のものが含まれる。
・原料(原薬出発物質、試薬、溶剤)
・中間体(最終中間体、一般中間体)
・助剤(ろ過助剤、活性炭など)
・製造材料(ガスケット、フィルターなど)
・包装材料(ボトル、栓、袋もの、乾燥剤、ドラム、ダンボールなど)
・表示材料(ラベル、識別材料など)
・原薬 等
発注先は、あらかじめ承認された原材料供給業者に限定される。
これは、同一品質の原材料入手体制の確立を目的とするものである。
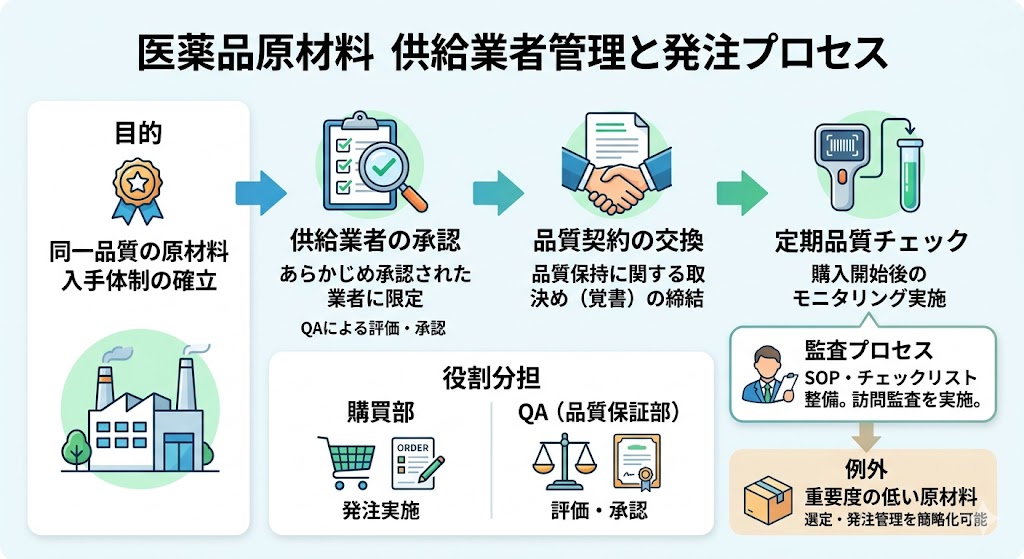
自社購買部の協力を得て実施し、供給業者の評価・承認はQAが実施する。
監査実施用のSOPおよびチェックリストを事前に整備し、必要に応じてトレーニングを受講した監査者が原材料供給業者への訪問監査を行う。
原材料供給業者とは品質保持に関する覚書(取決め)を交わし、購入開始後は定期的な品質チェックを実施する。
なお、製品品質への影響が少ない重要度の低い原材料については、供給業者の選定および発注管理を簡略化することが可能である。
原材料が入荷した際は、あらかじめ指定された入荷場所へ搬入し、受入れ検査を実施する。
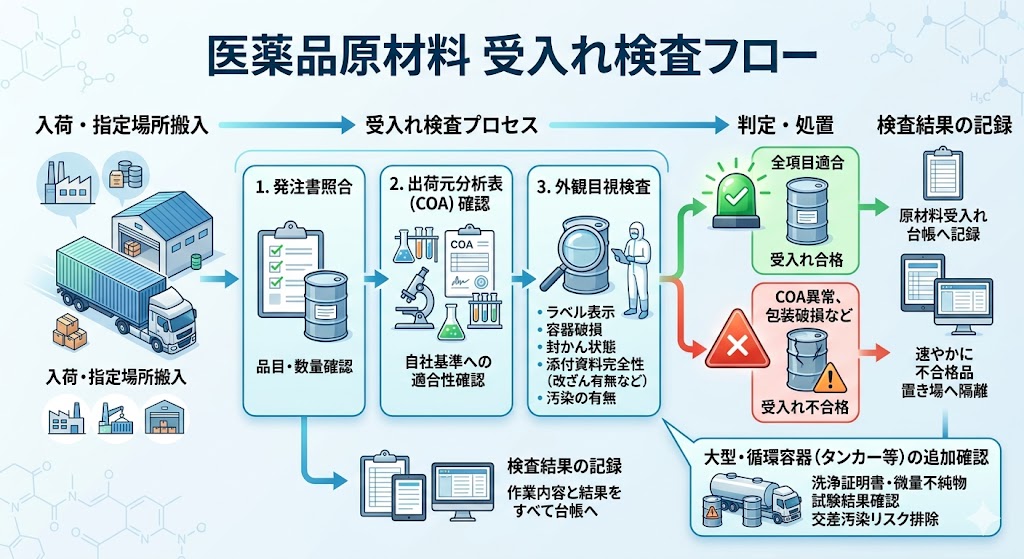
受入れ検査では、まず発注書との照合を行い、発注品との相違がないかを確認する。
続いて出荷元分析表(COA)の有無を確認し、記載された試験項目および試験結果が、自社の品質合格判定基準に適合していることを確認する。
さらに、出荷元のラベル表示、容器の破損や封かん状態、添付資料の完全性(改ざんの有無など)、汚染の有無について外観目視検査を実施し、すべての項目を満たした場合にのみ受入れ合格とする。
分析表の異常や包装材の破損等が発見された場合は受入れ不合格とし、誤使用を防止するため、速やかに不合格品置き場へ隔離する。
検査の合否に関わらず、ここまでの作業内容および結果はすべて「原材料受入れ台帳」に記録する。
タンカーやタンクローリー、循環利用されるドラムなどの大型容器のうち、専用容器でないものについては、洗浄証明書や微量不純物試験書の結果を確認する。前輸送物資との交差汚染が発生していないことを確認したうえで、受入れ作業を開始する。
【用語解説】
| QA(品質保証部) | Quality Assuranceの略。医薬品の品質が適切に保たれているかを第三者的な視点で評価・保証する部門。 |
|---|---|
| 出荷元分析表(COA) | Certificate of Analysisの略。原材料の製造元が製品の試験結果を記載し、品質規格に適合していることを証明する文書。 |
| 交差汚染(クロスコンタミネーション) | ある製品や原材料に、別の製品・物質や微生物が混入すること。医薬品製造において厳格に防ぐべき事象。 |
| 原薬 | 医薬品の有効成分となる物質。これに賦形剤などを加えて製剤化することで最終的な医薬品となる。 |
【ポイント】
1. リスクベースアプローチに基づく供給業者管理(サプライヤーマネジメント)
原材料の品質は最終製品の品質に直結するため、供給業者の評価・承認は形式的な手続きで終わらせてはならない。QAは、原材料が製品品質に与えるリスクの大きさに応じて、訪問監査の頻度や深度を調整する「リスクベースアプローチ」を採用すべきである。また、単なる覚書の交換にとどまらず、変更管理や逸脱発生時の報告義務を明記した厳格な品質取決め(GQP協定など)を締結し、継続的なモニタリングを行うことが不可欠である。
2. 共用設備・容器における交差汚染リスクの徹底排除
タンクローリー等の共用容器による輸送は、交差汚染リスクが極めて高い工程である。洗浄証明書の確認は必須であるが、書面上の確認のみに依存せず、洗浄バリデーションが適切に実施されているか、残留許容値の科学的根拠は妥当かを供給業者監査の段階で評価しておくべきである。万が一の汚染疑いが発生した際に迅速に原因究明ができるよう、トレーサビリティの確保と不合格品(リジェクト品)の物理的な隔離手順の徹底が現場の運用要件となる。