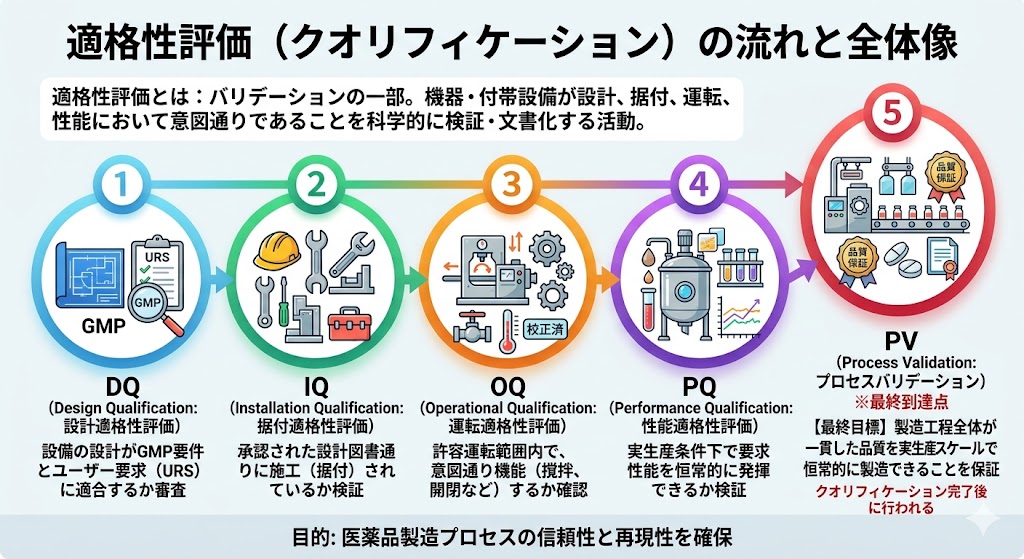
GQPとは!?
GQPとは…医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の方法を定めた基準であり、製造販売する製品の品質を確保するために必要な業務について定めたものである。
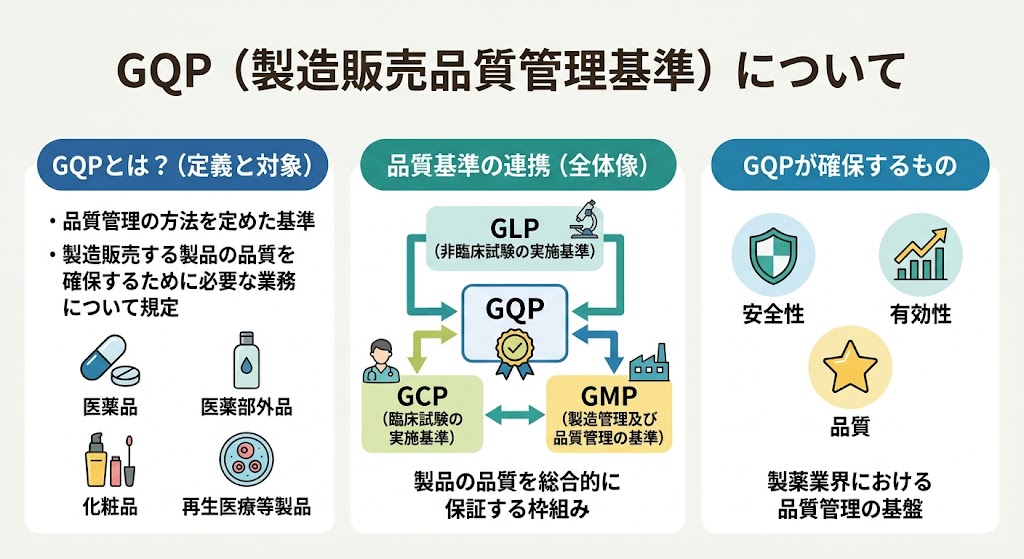
GQP(Good Quality Practice:製造販売品質管理基準)は、GMP(製造管理及び品質管理の基準)、GLP(非臨床試験の実施基準)、GCP(臨床試験の実施基準)などの各品質基準と連携し、製品の品質を総合的に保証する枠組みの一部である。製薬業界における品質管理の基盤を形成し、製品の安全性、有効性、および品質を確保するうえで不可欠な規範である。
以下に、GQPにおける重要なポイントを3つ挙げる。
医薬品においては、製造所が独自の基準でいかに厳密な最終試験や検査を実施したとしても、それだけで製造販売を行うことは許可されない。
GQPは、薬機法(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律)に基づき「医薬品、医薬部外品、化粧品及び医療機器の品質管理の基準」として定められており、本基準に適合しなければ製品を市場へ供給することはできない。
具体的には、製品を市場へ出荷する際の判定基準や手順など、品質管理業務を適切に実施するためのルール構築、ならびにその実施の監督を通じ、市場出荷に対する最終的な責任を負うことが規定されている。
GQPにおいては、製造販売業の許可要件として、以下の内容に関する手順書等の文書作成が義務付けられている。
【第1種医薬品製造販売業】
【第2種医薬品製造販売業、又はGMP対象製品を扱う医薬部外品製造販売業】
〇 品質標準書
〇 品質管理業務の手順に関する文書
・市場への出荷の管理
・適正な製造管理及び品質管理の確保
・品質等に関する情報及び品質不良等の処理
・回収処理
・自己点検
・教育訓練
・製品の貯蔵等の管理
・文書及び記録の管理
・安全管理統括部門その他の品質管理業務に関係する部門又は責任者との相互の連携
・その他、品質管理業務を適正かつ円滑に実施するために必要な業務
【医薬部外品(GMP対象外)、又は化粧品製造販売業】
・品質管理業務の手順に関する文書
・市場への出荷に係る記録の作成
・適正な製造管理及び品質管理の確保
・品質等に関する情報及び品質不良等の処理
・回収処理
・文書及び記録の管理
・その他、品質管理業務に関する事項
(補足)
自己点検および教育訓練については、各企業が必要に応じて実施することが推奨される。
これらの文書では、出荷判定基準、製造所における製造管理および品質管理の確保の方法、品質に関する苦情処理の手順などを定めており、GQPはGVP(製造販売後安全管理基準)とともに製造販売業の重要な許可要件となっている。
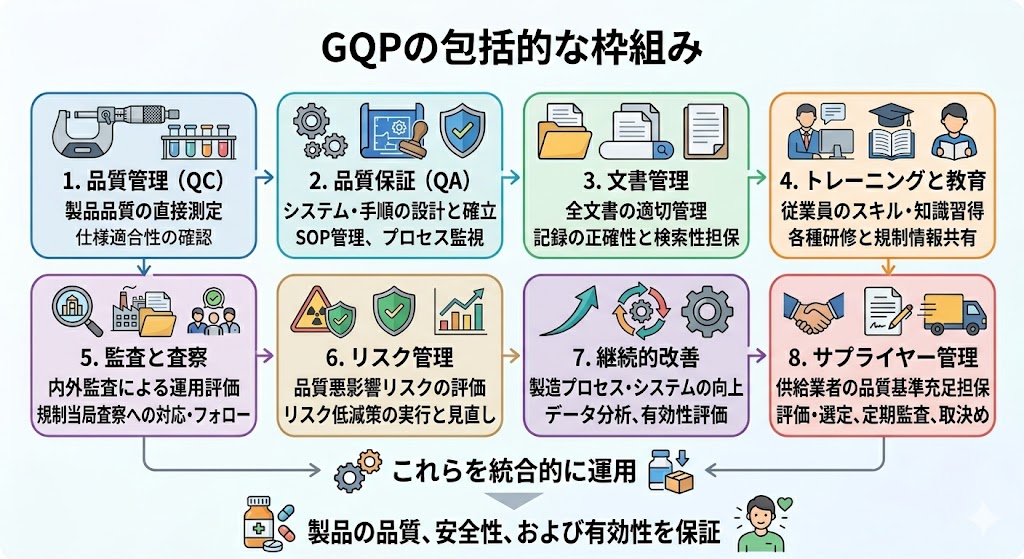
1. 品質管理(Quality Control, QC)
製品の品質を直接測定し、仕様に適合しているかを確認する。
原材料、製造中間体、最終製品の検査および試験、試験結果の記録と分析、不適合品の処理および再試験などを実施する。
2. 品質保証(Quality Assurance, QA)
製品が一貫して品質基準を満たすことを担保するためのシステムや手順を設計、導入、維持する。
標準作業手順書(SOP)の作成と管理、製造プロセスの監視および評価、内部品質監査の実施、継続的改善の推進などを担う。
3. 文書管理(Document Management)
製品やプロセスに関するすべての文書を適切に管理し、必要な情報が正確に記録され、かつ検索・アクセス可能であることを保証する。
製造記録の維持、試験記録と分析結果の保存、変更管理の文書化などを実施する。
4. トレーニングと教育(Training and Education)
従業員が必要なスキルと知識を習得し、GQPに基づいた業務を遂行できるようにする。
新規従業員の初期研修、継続的なスキルアップとリフレッシュ研修、最新の規制情報の共有と教育などを実施する。
5. 監査と査察(Audits and Inspections)
内部および外部の監査を通じて、GQPが適切に運用されているかを評価し、改善点を特定する。
定期的な内部監査の実施、第三者機関による品質監査の受審、規制当局による査察への対応およびフォローアップなどを実施する。
6. リスク管理(Risk Management)
製品の品質に悪影響を及ぼす可能性のあるリスクを評価し、適切に管理する。
リスクの評価と分析、リスク低減策の立案と実行、リスク管理活動の文書化および定期的な見直しなどを実施する。
7. 継続的改善(Continuous Improvement)
製造プロセスおよび品質システムの継続的な改善を促進する。
データの傾向分析(トレンド分析)、改善策の立案と実行、改善活動の有効性評価などを実施する。
8. サプライヤー管理(Supplier Management)
原材料や中間製品の供給業者(サプライヤー)が、要求される品質基準を確実に満たしていることを担保する。
サプライヤーの評価および選定、定期的な監査、取決め(品質保証協定など)の締結および管理を実施する。
これらの要素を統合的に運用することで、GQPは製品の品質、安全性、および有効性を強固に保証している。
【用語解説】
| GQP | Good Quality Practiceの略。医薬品や化粧品などの品質管理の方法を定めた基準。 |
|---|---|
| GMP | Good Manufacturing Practiceの略。医薬品等の製造管理および品質管理の基準。製造所の構造設備や作業手順等を定める。 |
| GLP | Good Laboratory Practiceの略。医薬品の安全性に関する非臨床試験(動物実験など)の実施基準。 |
| GCP | Good Clinical Practiceの略。医薬品の臨床試験(治験)を実施する際の基準。 |
| GVP | Good Vigilance Practiceの略。製造販売後の医薬品等の安全管理(副作用情報の収集や評価など)に関する基準。 |
| 薬機法 | 「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」の略称。医薬品等の製造、販売、安全対策などを規制する。 |