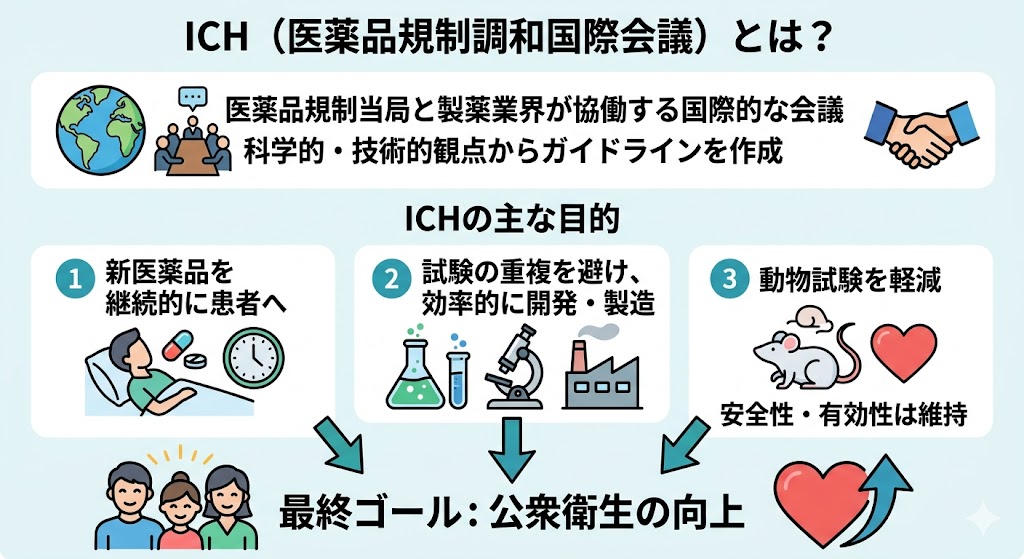
�i���Ɋւ���K�C�h���C���uICH Q1�`Q14�v�Ƃ́I�H
�@ICH�ł́AISO�̍l�������x�[�X�Ɉ��i�ƊE���L�̗v�f�������ꂽ�i���V�X�e���̃K�C�h���C�����쐬���A���\���Ă���B
�@�i���Ɋւ���K�C�h���C���́AICH Q1����n�܂�A2026�N5�����݂ł�ICH Q1�`Q14�܂ō��肳��Ă���B
�@�����J���Ȃ���ʒm����A�����K���Ƃ��ē����ς��i�X�e�b�v5�j�ƂȂ��Ă����ȃK�C�h���C���i2026�N���_�j���ȉ��Ɏ����B
| �K�C�h���C�� | �K�C�h���C���̎�ȓ��e | �ʒm���E �֘A�����N |
|---|---|---|
Q1 |
�y���萫�z ��Q1A�iR2�j�u���萫�����K�C�h���C���v�� ��Q1B�u�V����y�ѐV���܂̌����萫�����K�C�h���C���v�� ��Q1C�u�V���^�o�H���i���̈��萫�������т̎戵���Ɋւ���K�C�h���C���v�� ��Q1D�u����y�ѐ��܂̈��萫�����ւ̃u���P�b�e�B���O�@�y�у}�g���L�V���O�@�̓K�p�v�� ��Q1E�u���萫�f�[�^�̕]���Ɋւ���K�C�h���C���v�� ��Q1F�u�C����III�y��IV�ɂ����鏳�F�\���̂��߂̈��萫�������тɊւ���K�C�h���C���v�̔p�~�� |
2003.6.3 1997.5.28 1997.5.28 2002.7.31 2003.6.3 2006.7.3
Q1F�p�~�ʒm |
Q2 |
�y���͖@�o���f�[�V�����z ��Q2�iR1�j�u���͖@�o���f�[�V�����Ɋւ���e�L�X�g�i���{���ځj�v�� ��Q2�iR1�j�u���͖@�o���f�[�V�����Ɋւ���e�L�X�g�i���{���@�j�v�� |
1995.7.20 1997.10.28
���{���@���� |
Q3 |
�y�s�����z �@��Q3A�iR2�j�u�V�L�������ܗL���i�̂�������̕s�����Ɋւ���K�C�h���C���v�� �B��Q3B�iR2�j�u�V�L�������ܗL���i�̂������܂̕s�����Ɋւ���K�C�h���C���v�� �D��Q3C�iR3�`R6�j�u���i�̎c���n�}�K�C�h���C���v�y�ъe������ �I��Q3D�u���i�̌��f�s�����K�C�h���C���ɂ��āv�� |
2002.12.16 2003.6.24 1998.3.30 2015.9.30
�I���� |
Q4 |
�y��Ǖ��z ��ICH Q4B �K�C�h���C���i��Ǖ��e�L�X�g��ICH�n��ɂ����đ��ݗ��p���邽�߂̕]���y�ъ����j�� ���eAnnex�i�����ʕt�������j�� |
2009.5.26 2009.5.26
Annex 1���� �i����Annex��PMDA�����Q�Ɓj
|
Q5 |
�y������i�̕i���z ��ICH Q5A�iR1�j�u�E�C���X���S���]���v�� ��ICH Q5B�u��`�q�����\���̂̕��́v�� ��ICH Q5C�u������i�̈��萫�����v�� ��ICH Q5D�u�זE��܂̗R���A�����y�ѓ�����́v�� ��ICH Q5E�u�����H���̕ύX�ɂƂ��Ȃ��������^�������]���v�� |
2000.2.22 1998.1.6 1998.1.6 2000.7.14 2005.4.26
Q5E���� |
Q6 |
�y�K�i����ю������@�z ��ICH Q6A�u�V���i�̋K�i�y�ю������@�̐ݒ�v�� ��ICH Q6B�u������i�̋K�i�y�ю������@�̐ݒ�v�� |
2001.5.1 2001.5.1
Q6B���� |
Q7 |
�y����GMP�̃K�C�h���C���z �E����i���i�̗L�������j�Ɋւ��鐻���Ǘ��y�ѕi���Ǘ��iGMP�j�̍��ۓI�ȕW����������Ă���B |
2001.11.2 2016.3.8
Q&A���� |
Q8 (R2) |
�y���܊J���z �E���i����ѐ����H���̊J���ɑ���A�Ȋw�ƃ��X�N�Ɋ�Â��A�v���[�`�iQuality by Design�FQbD�j���L�q���Ă���B |
2010.6.28 ���� |
Q9 |
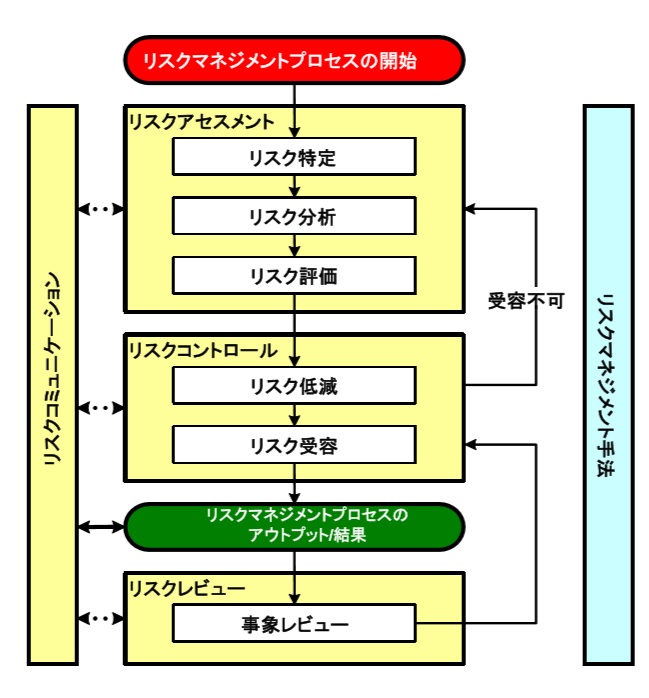
�y�i�����X�N�}�l�W�����g�z �E���i���C�t�T�C�N���S�̂�ʂ����A�i���ɑ��郊�X�N�̃A�Z�X�����g�A�R���g���[���A�R�~���j�P�[�V�����A����у��r���[�̌n���I�v���Z�X���L�q���Ă���B
|
2006.9.1 ���� |
Q10 |
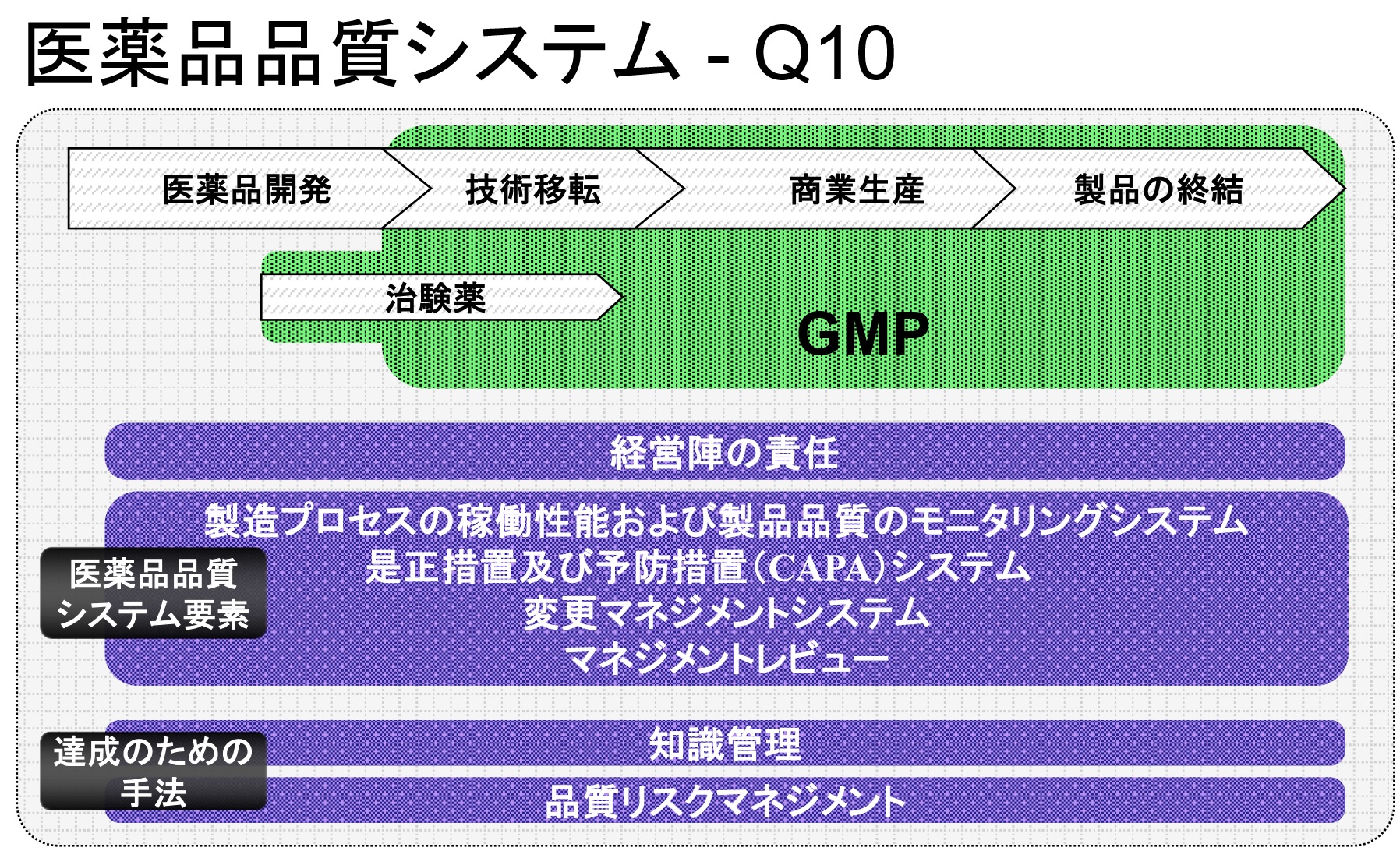
�y���i�i���V�X�e���iPQS�j�z �E�K�ȕi��������L���鐻�i���P��I�ɋ������邽�߂̃V�X�e���m���E�ێ��ɂ��ċL�q���Ă���B |
2010.2.19 ���� |
Q11 |
�y����̊J���Ɛ����i���w�����^�����N���R�������j�z �EICH Q8�AQ9�AQ10�̌����ƊT�O�iQ�g���I�j���A����̊J���Ɛ����Ɋ֘A�Â��Đ������Ă���B |
2014.7.10 ���� |
Q12 |
�y���i���C�t�T�C�N���}�l�W�����g�iPLCM�j�z �E���i�̃��C�t�T�C�N���}�l�W�����g�ɂ�����Z�p��y�ыK����̍l�����Ɋւ���K�C�h���C���B |
2021.10.29 �֘A��� |
Q13 |
�y����y�ѐ��܂̘A�����Y�z �E����ѐ��܂̘A�����Y�̊J���A�����A����у��C�t�T�C�N���}�l�W�����g�Ɋւ���Ȋw�I�E�K����̍l�����������Ă���B |
2023.5.31 �֘A��� |
Q14 |
�y���͖@�̊J���z �E���͖@�J���ɂ�����Ȋw�I�A�v���[�`�i���͖@���C�t�T�C�N���}�l�W�����g�̊T�O�Ȃǁj�������A��茘�S�ȕ��͖@�̊J���𑣐i����B |
2025.10.9 �֘A��� |
�y�|�C���g�z
1. Q12�`Q14�����ɂ��u�J������A�����Y�܂ł̃��C�t�T�C�N���Ǘ��v�̍��x��
�ߔN���o���ꂽQ12�i���i���C�t�T�C�N���}�l�W�����g�j�AQ13�i�A�����Y�j�AQ14�i���͖@�̊J���j�ɂ��A���i�̕i���Ǘ��͐V���ȃX�e�[�W�ɓ˓����Ă���B����Q12��PACMP�i���F��ύX�Ǘ����{�v�揑�j�����p���邱�ƂŁA���O�̃��X�N�]���Ɋ�Â����_��ȕύX�Ǘ����\�ƂȂ�A�t�ܒ�����[�U�Ƃ�������������̃v���Z�X���P��v���ɐi�߂₷���Ȃ����B�܂��AQ13�������A�����Y��AQ14�����߂錘�S�ȕ��͖@�́A���A���^�C���ł̕i���ۏ�O��Ƃ��Ă��邽�߁A�@��̃I�[�f�B�b�g�g���C�����܂߂���茵�i�ȃf�[�^�C���e�O���e�B�iDI�j�Ή������߂���B
2. Q�g���I�iQ8, Q9, Q10�j���甭�W�����p���I���P�̃T�C�N���\�z
Q12�ȍ~�̐V�����K�C�h���C���Q�́A������Q8�i���܊J���j�AQ9�i�i�����X�N�}�l�W�����g�j�AQ10�i���i�i���V�X�e���j�Ƃ������uQ�g���I�v�̊�Ղ̏�ɐ��藧���Ă���B�K�C�h���C����P�Ȃ�K���Ƃ��đ�����̂ł͂Ȃ��A�������I���헪�I�ɉ^�p���A��E�������ɂ͍��{���������Ɋ�Â�CAPA�i�����[�u�E�\�h�[�u�j���m���ɋ@�\�����邱�Ƃ��d�v�ł���B���̈�A�̃V�X�e�������ꃌ�x���Œ蒅�����邱�Ƃ��A���苟���̈ێ���i���s�ǂ̖��R�h�~�ɒ�������B
�@