医薬品製造に関わる基礎知識をまとめて紹介します。薬機法改正についてまとめました。
日本の医薬品の法体系とは!?
日本の医薬品製造に係る法体系は次図のようになっている。
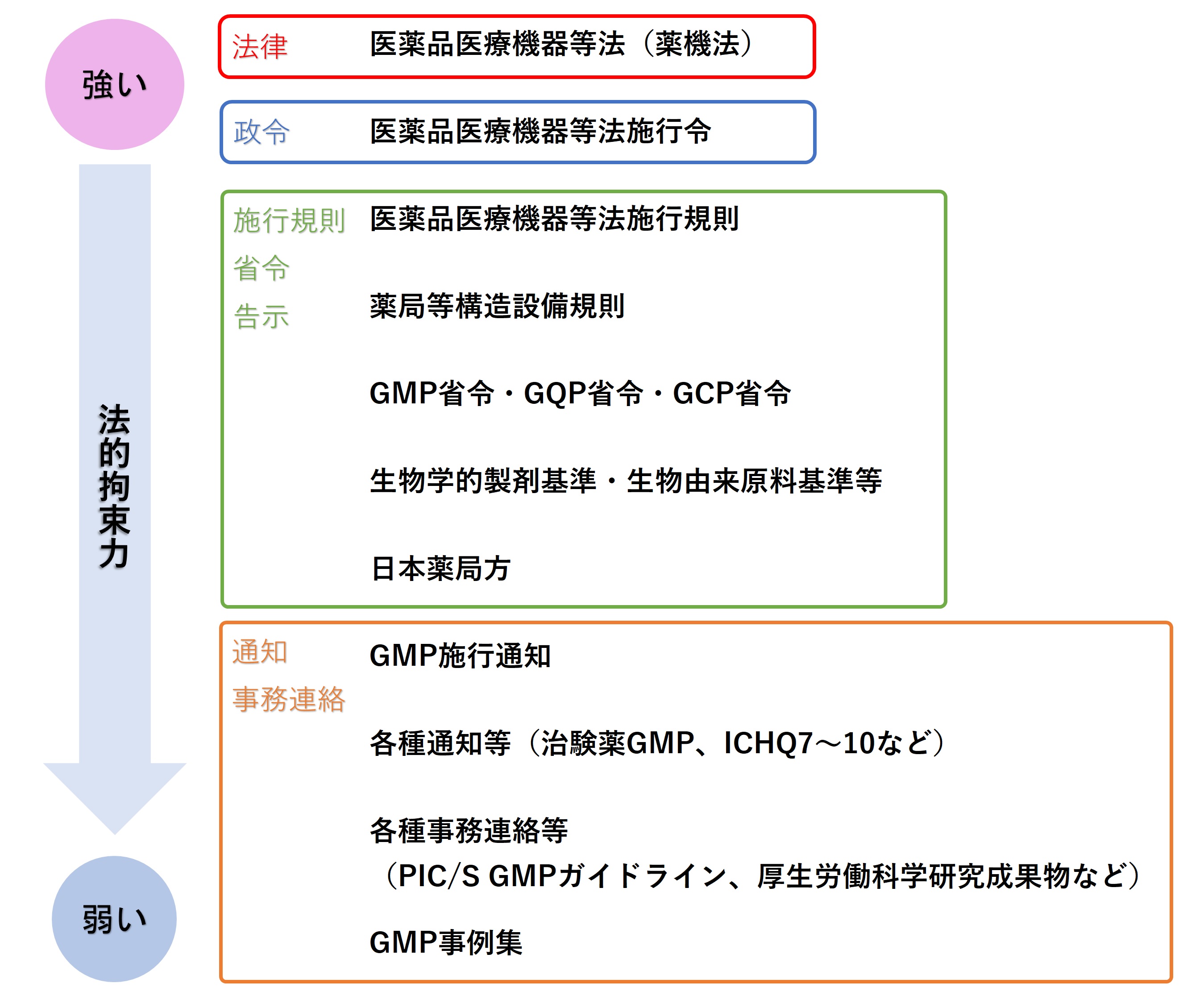
薬機法の法的拘束力
医薬品製造に係る法体系で、薬機法が一番法的拘束力が強い。
薬機法は、正式名称を「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」といい、昭和23(1948)年に「薬事法」として制定されて以降、現在に至るまでさまざまな改正を重ねてきた法律である。
現在の正式名称に題名が改められたのは平成25(2013)年の改正によるもので、略称としては「薬機法」のほか、「医薬品医療機器等法」と呼ばれることがある。
GMPは、薬機法に基づく法令要件である。
医薬品の法体系における「法律」「政令」「省令」「規則」「通知」の違い
医薬品の法体系における「法律」「政令」「省令」「規則」「通知」の違いについて次に示す。
【各分類の説明】
| 法律 |
|---|
| 日本の法体系の最上位に位置する。例えば、「医薬品医療機器等法(薬機法)」は、医薬品や医療機器の製造・販売・使用に関する基本的な枠組みを定めている。法律改正には国会の承認が必要であり、手続きが厳格である。 |
| 政令 |
| 法律を具体的に実施するために必要な細かい規定を定める。例えば、「薬機法施行令」は、薬機法で定められた内容を施行するための細部を補足している。政令は内閣が制定するため、国会の承認は不要だが、法律の範囲内でしか制定できない。 |
| 省令 |
| 厚生労働省などの行政機関が、法律や政令に基づいて運用上必要な詳細を定める。医薬品分野では、GMP省令や医薬品製造販売業の基準などがこれに該当する。省令は実務的な運用指針としての役割が強く、頻繁に改正される場合もある。 |
| 規則 |
| 業界団体や関係機関が定める具体的な基準やルール。例えば、製造現場における詳細な運用基準や、品質管理の具体的な手順が規則として定められることがある。実務的な指針として現場で活用されることが多い。 |
| 通知 |
| 法律や省令を解釈した運用指針を示し、行政や業界に実務の指標を提供。 |
【各分類の違い】
| 分類 | 特徴 | 制定主体 | 具体例(医薬品分野) |
|---|---|---|---|
| 法律 | ・国会で制定される最上位の法規範 ・国全体に適用される基本的なルール ・下位規範(政令、省令)に指針を与える |
国会 | ・医薬品医療機器等法(薬機法) ・健康保険法 |
| 政令 | ・法律を施行するための詳細な規定を定める ・法律の範囲内で作成される ・必要に応じて柔軟に改正可能 |
内閣 | ・医薬品医療機器等法施行令 ・健康保険法施行令 |
| 省令 | ・各省庁が政令や法律に基づいて細かい運用規則を定める ・専門的な分野や実務的なルールを補足 |
厚生労働省などの行政機関(医薬品の場合) | ・医薬品医療機器等法施行規則 ・GMP省令(医薬品の製造管理および品質管理基準) |
| 規則 | ・更に具体的な基準やガイドラインを示す ・業界や特定の分野に適用されるルールを定める |
厚生労働省などの行政機関 | ・医薬品品質管理基準(日本薬局方に基づく) ・特定医薬品の流通管理規則 |
| 通知 | ・行政機関からの指針や解釈を示した文書 ・法的拘束力はないが、実務上重要 |
厚生労働省などの行政機関 | ・医薬品の適正使用に関する通知 ・GMPガイドライン通知 |
このように日本の医薬品の法体系は、「法律」を最上位とし、「政令」「省令」「規則」「通知」がそれを補完する形で階層的に構成されている。
この階層的な仕組みにより、医薬品の安全性と適正利用が支えられている。
厚生労働省の改正薬機法資料はこちら
厚生労働省「薬機法全文」はこちら


