�s�������̎���i�������܂̐����L�^�U���j
�@M�����Ђ́A����̗A���E�̔��A�����̐����E�̔����肪����ق��A���N�H�i�̐����E�̔��̐���������W�J���Ă���B
�@�Q�O�P�X�N�A���̏��F���e�ƈقȂ鐻�����@�Ŋ������G�L�X�Ȃ�117�i�ڂ̊������܂����A�����L�^���U������Ȃǂ��āA������34���Ԃ̋Ɩ���~�����𖽂���ꂽ�B
�@�������S�ۂɂ��ƁA���ۈ��Ă̓����̒ʕ����AM�����ЍH��ւ̗������������{���A�����Ǘ��̕s���������B
�@���̌�A�����Ǘ��Ɋւ�����P�Əo�ςݐ��i�̌����s�����ŁA���i117�i�ڂŌ��J�Ȃ̏��F���e�ƈقȂ鐻�������������Ƃ������B
�@����ɁA���̂��Ƃ����o���Ȃ��悤�����Ɋւ���L�^���U�����A�Ď����ɑ��Ă����U�̓������s���Ă����������m�F�����B
�@��������292�i�ڂɂ��āA�����L�^�E�����L�^���̒������s�������ʁA����3�_���m�F����A130�i�ڂɂ����Ď��������̕K�v�ȑ[�u���s�����B
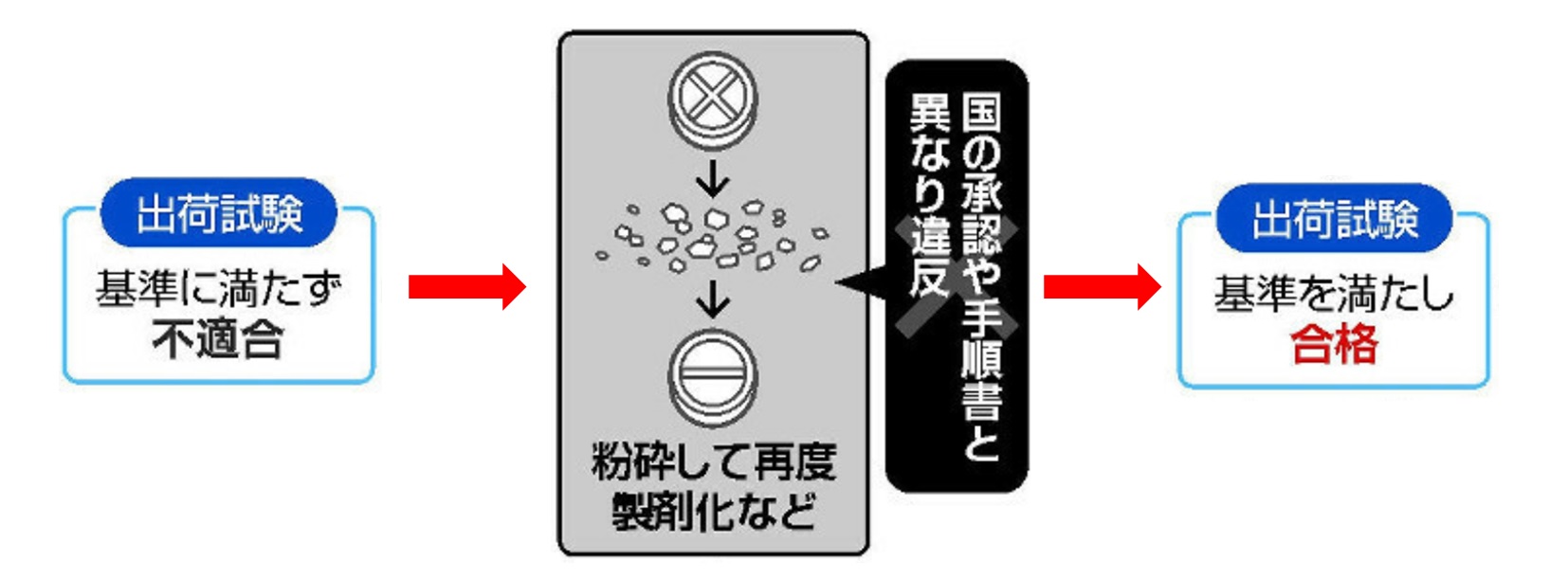
�E���F�����قȂ鐻�����@�ɂ�鐻�����s���Ă���
�E���F���ƈقȂ鐻�����s������ŁA�s�K�ȋL�^�Ǘ����s���Ă���
�E�����L�^���������m�F���ꂽ
�@�H��ɂ�����L�^�Ǘ��Ɋւ���s���̔��������́A���L��4�_�Ƃ��Ă���B
�@�Ǘ��\�͂��������i�ڐ��ƂȂ��Ă�������
���ЂŊǗ��ł��鋖�e�͈͂����i�ڐ��ƂȂ��Ă���A�K�ȊǗ����s���Ȃ���Ԃ������B
�AGMP���[���̏�����[����D�悷��l����������
�[�����ŗD�悷�邪���܂�AGMP���[������̈ӂɈ�E���A�����H�����ȗ�����s�ׂ������̕i�ڂŔ��������B
�B���F�����e�ɂ��Ă̕K�v�Ȍ��A�葱����ӂ���
�J���i�K��������Y�ւ̍H�Ɖ��������s�\���A�܂��́A���F���ʂ�̐������@�ł͎����Y���ł��Ȃ��c�݂������Ă����B
�C�g�D�Ƃ��ăR���v���C�A���X�ӎ��̌��@
�ߋ�����̕s���s�ׂɂ���āA��E�҂��܂߂ĊW�]�ƈ��̕s���ɑ���ӎ��������A�܂��A�s���̏�ԉ��ɂ���Ă�����B�����邱�Ƃɑ���߈������ƂȂ�A���Ղɖ@�菑�ނ̋U�����s�����B
�@���Ђ́A���i�����̔��ƂƂ��āA�ᔽ���e�̉��P���܂߁AGQP�ȗ߁A���̑��̊W�@�߂����炷��悤�Ɩ����P�����{����Ƃ��Ă���B
�@